
 正丁醚(CH3CH2CH2CH2OCH2CH2CH2CH3)是一种化工原料,常温下为无色液体,不溶于水,沸点为142.4℃,密度比水小.某实验小组利用如下装置合成正丁醚(其它装置均略去),发生的主要反应为:2C3CH2CH2CH2OH$→_{135°}^{浓H_{2}SO_{4}}$CH3CH2CH2CH2OCH2CH2CH2CH3+H2O
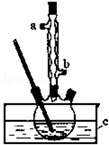
正丁醚(CH3CH2CH2CH2OCH2CH2CH2CH3)是一种化工原料,常温下为无色液体,不溶于水,沸点为142.4℃,密度比水小.某实验小组利用如下装置合成正丁醚(其它装置均略去),发生的主要反应为:2C3CH2CH2CH2OH$→_{135°}^{浓H_{2}SO_{4}}$CH3CH2CH2CH2OCH2CH2CH2CH3+H2O分析 在容积为100mL的三颈烧瓶中将5mL浓硫酸、14.8g正丁醇和几粒沸石混合均匀,再加热回流一段时间,收集到粗产品,精制得到正丁醚,
(1)浓硫酸与其它液体混合时,先加其它液体后加硫酸;
(2)用冷凝管冷凝时,冷凝水的流向与气体流向相反;
(3)液体能达到的最高温度等于其沸点;
(4)浓硫酸被还原生成二氧化硫,用氢氧化钠溶液吸收二氧化硫;
(5)分离分层的液体用分液漏斗;带有玻璃塞的仪器使用前要检漏;
(6)有机物易挥发;
(7)产率=$\frac{实际产量}{理论产量}$×100%.
解答 解:(1)浓硫酸与其它液体混合时,先加其它液体后加硫酸,防止浓硫酸稀释时放热,引起液体飞溅,所以液体试剂加入顺序是先加正丁醇,后加浓硫酸,
故答案为:先加正丁醇,后加浓硫酸;
(2)用冷凝管冷凝时,冷凝水的流向与气体流向相反,则冷凝水从a口进入,
故答案为:a;
(3)加热液体能达到的最高温度等于其沸点,则为保证反应温度恒定在135℃,装置C中所盛液体的沸点应该大于135℃,
故答案为:该液体沸点大于135℃;
(4)加热时间过长或温度过高,反应混合液会变黑,浓硫酸与丁醇发生氧化还原反应,浓硫酸被还原生成二氧化硫,用氢氧化钠溶液吸收二氧化硫,其二氧化硫与氢氧化钠的反应离子方程式为:2OH-+SO2═SO32-+H2O;
故答案为:2OH-+SO2═SO32-+H2O;
(5)分离分层的液体用分液漏斗,该步骤中需要的属于硅酸盐材质的实验仪器是烧杯、玻璃棒、分液漏斗;带有玻璃塞的仪器使用前要检漏,则在使用分液漏斗时要先检验是否漏水;
故答案为:分液漏斗;检验是否漏水;
(6)将分离出的有机层用无水氯化钙干燥,正丁醚易挥发,采用蒸馏的方法获得纯净的正丁醚,
故答案为:蒸馏;
(7)由2CH3CH2CH2CH2OH$→_{135℃}^{浓硫酸}$CH3CH2CH2CH2OCH2CH2CH2CH3+H2O,
74×2 130
14.8g mg
则m=$\frac{14.8g×130}{74×2}$=13.0g
产率=$\frac{实际量}{理论量}$×100%=$\frac{6.5g}{13.0g}$×100%=50.0%,
故答案为:50.0%.
点评 本题考查有机化学实验、反应原理、基本操作、化学计算等,题目难度中等,注意把握常见实验操作、尾气处理、仪器使用,注意对基础知识的理解掌握.


科目:高中化学 来源: 题型:选择题
| A. | 2v正(B)=v逆(C) | B. | 该体系的密度都不随时间变化 | ||
| C. | 1molA断裂,同时1molC也断裂 | D. | 该体系的温度不随时间而变化 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
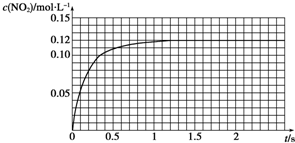
| 序号 | 反应温度/℃ | c(H2O2)/mol•L-1 | V(H2O2)/mL | m(MnO2)/g | t/min |
| 1 | 20 | 2 | 10 | 0 | t1 |
| 2 | 20 | 2 | 10 | 0.1 | t2 |
| 3 | 20 | 4 | 10 | 0.1 | t3 |
| 4 | 40 | 2 | 10 | 0.1 | t4 |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
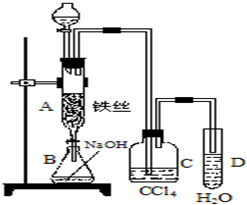 某化学课外小组用如图装置制取溴苯.先向分液漏斗中加入苯和液溴,再将混合液慢慢滴入反应器A(A下端活塞关闭)中.
某化学课外小组用如图装置制取溴苯.先向分液漏斗中加入苯和液溴,再将混合液慢慢滴入反应器A(A下端活塞关闭)中.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
 N和Si是合成新型非金属材料的两种重要元素.请回答:
N和Si是合成新型非金属材料的两种重要元素.请回答: ;Si原子可形成多种氢化物,其中Si2H6中Si原子的价层电子对数目为4.
;Si原子可形成多种氢化物,其中Si2H6中Si原子的价层电子对数目为4.查看答案和解析>>
科目:高中化学 来源: 题型:实验题
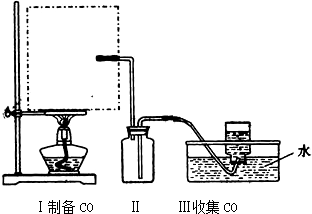
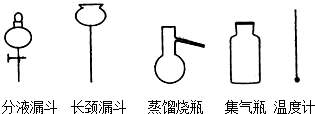
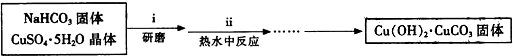
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 温度/℃ | 0 | 10 | 30 | 50 | 56.7 | 60 | 64 | 70 | 80 | 90 | ||
| 溶解度/g | 14.0 | 17.0 | 25.0 | 33.0 | 35.2 | 35.3 | 35.6 | 33.0 | 30.5 | 27.0 | ||
| 析出晶体 | FeSO4•7H2O | FeSO4•4H2O | FeSO4•H2O | |||||||||
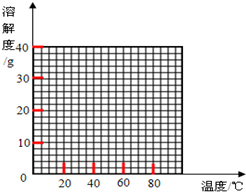
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com