
| 化合物 | PbSO4 | PbCO3 | PbS |
| 溶解度/g | 1.03×10-4 | 1.81×10-7 | 1.84×10-14 |
科目:高中化学 来源:不详 题型:单选题
| A.Na2CO3水溶液呈碱性,所以其热溶液可以除去物品表面的油污 |
| B.Fe(OH)3胶体能吸附水中的悬浮颗粒并沉降,因而具有净水作用 |
| C.氯化亚铁溶液与无色的KSCN溶液混合,溶液不呈红色 |
| D.SO2通入品红溶液,红色褪去,再加热,红色不再出现 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.BaSO4比BaCO3溶解度小,所以,BaCO3可以转化为BaSO4 |
| B.BaCO3、BaSO4均不溶于水,所以都可以做钡餐试剂 |
| C.向Na2CO3溶液中加入BaCl2和Na2SO4,当两种沉淀共存时,c(SO42—)/ c(CO32—) =4.4×10-2 |
| D.常温下,BaCO3若要在Na2SO4溶液中开始转化为BaSO4,则Na2SO4的浓度必须不低于2.2×10-6 mol·L-1 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| 选项 | ① | ② | ③ | 实验结论 | 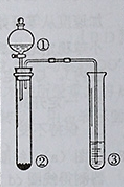 |
| A | 稀硫酸 | Na2S | AgNO3与AgCl的浊液 | Ksp(AgCl)>Ksp(Ag2S) | |
| B | 浓硫酸 | 蔗糖 | 溴水 | 浓硫酸具有脱水性、氧化性 | |
| C | 稀盐酸 | Na2SO3 | Ba(NO3)2溶液 | SO2与可溶性钡盐均可以生成白色沉淀 | |
| D | 浓硝酸 | Na2CO3 | Na2SiO3溶液 | 酸性:硝酸>碳酸>硅酸 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:问答题

| 物质 | 开始沉淀 | 沉淀完全 |
| Fe(OH)3 | 2.7 | 3.7 |
| Cu(OH)2 | 5.6 | 6.7 |
| Al(OH)3 | 3.8 | 4.7 |
 CuOH + H+的平衡常数为: 。
CuOH + H+的平衡常数为: 。查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.氨水 | B.硫化氢气体 |
| C.硫酸钠溶液 | D.纯碱溶液 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题

 2CrO42-(黄色)+ 2H+,此时溶液应呈现的颜色是 。
2CrO42-(黄色)+ 2H+,此时溶液应呈现的颜色是 。| 物质 | Fe(OH)3 | Al(OH)3 | Cr(OH)3 | Fe(OH)2 | Mg(OH)2 |
| 开始沉淀 | 1.5 | 3.4 | 4.9 | 6.3 | 9.6 |
| 完全沉淀 | 2.8 | 4.7 | 5.5 | 8.3 | 12.4 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com