
【题目】亚硝酰氯(NOCl)是有机物合成中的重要试剂,为红褐色液体或黄色气体,室温下为不稳定的黄色气体, 具刺鼻恶臭味,遇水分解,某学习小组用 C12 和 NO 制备 NOCl 装置如图。下列说法错误的是
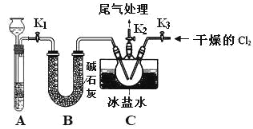
A.氯气在反应中做氧化剂
B.装入药品后,要先打开 K2、K3,反应一段时间后,再打开 K1
C.利用 A 装置还可以做 Na2O2 和水制氧气的实验
D.若没有 B 装置,C 中可能发生反应:2NOCl+H2O=2HCl+NO↑+NO2↑
【答案】C
【解析】
由装置A制备NO,用铜和稀硝酸反应制备,制得的NO中可能有挥发的硝酸,故装置B用来净化和干燥NO,将氯气和NO干燥后在装置C中发生反应,在冰盐中冷凝收集NOCl,氯气、NO以及NOCl均不能排放到空气中,用氢氧化钠溶液吸收,NOCl遇水易水解,故在收集装置和尾气处理装置之间应该需加一个干燥装置。
A. 根据Cl2和NO反应生成了NOCl,氯元素化合价降低,得电子,Cl2为氧化剂,故A正确;
B. 先打开K2、K3,通入一段时间氯气,排尽三颈烧瓶中的空气,防止NO、NOCl 变质,然后再打开K1,通入NO,故B正确;
C. 该装置能制备用块状固体和液体反应生成的气体,过氧化钠为粉末状固体,所以不可以做Na2O2和水制氧气的实验,故C错误;
D. 若无装置B,C中亚硝酰氯与水反应生成氯化氢、NO和二氧化氮,可能发生反应:2NOCl+H2O═2HCl+NO↑+NO2↑,故D正确;
故选:C。


科目:高中化学 来源: 题型:
【题目】已知某种有机物A的质谱图和红外光谱图如图,以下说法正确的是( )
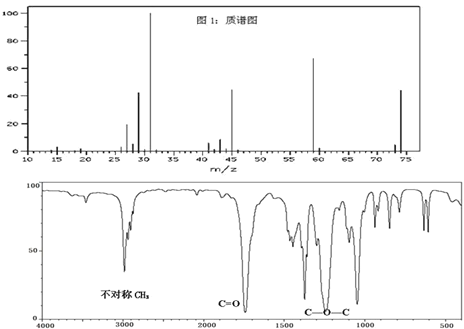
A.由质谱图可知,有机物A的摩尔质量为74
B.由红外光谱可知,有机物A的分子式C3H6O2
C.有机物A的核磁共振氢谱图中有3种吸收峰,峰面积之比为1:2:3
D.有机物A的名称为甲酸乙酯,官能团为酯基
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】六氟化硫(SF6)分子为正八面体构型(分子结构如图所示),难溶于水,在高温下仍有良好的绝缘性,在电器工业方面具有广泛用途。下列推测正确的是( )
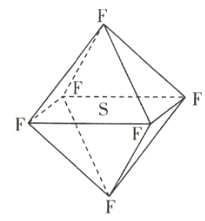
A.SF6各原子均达到最外层8电子稳定结构
B.SF6易燃烧生成SO2
C.SF6分子是含有极性键的非极性分子
D.SF6是原子晶体
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一种芳纶纤维的拉伸强度比钢丝还高,可广泛用作防护材料。该高分子化合物的结构片段如图所示。下列说法正确的是( )
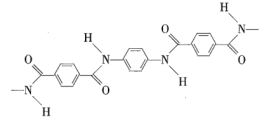
A.羊毛与芳纶纤维的主要化学成分相同
B.该高分子化合物的结构简式为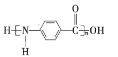
C.该高分子化合物完全水解产生的单个分子中,每个分子苯环上的氢原子都具有不同的化学环境
D.通过质谱法测定芳纶纤维的平均相对分子质量,可得其聚合度
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】甲酸(化学式HCOOH,分子式CH2O2,相对分子质量46),俗名蚁酸,是最简单的羧酸,无色而有刺激性气味的易挥发液体。熔点为8.6 ℃,沸点100.8℃,25℃电离常数Ka=1.8×10-4。某化学兴趣小组进行以下实验。
Ⅰ.用甲酸和浓硫酸制取一氧化碳
A. 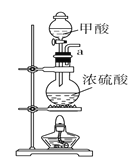 B.
B. 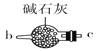 C.
C. 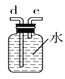 D.
D. 
(1)请说出图B中盛装碱石灰的仪器名称__________。用A图所示装置进行实验。利用浓硫酸的脱水性,将甲酸与浓硫酸混合,甲酸发生分解反应生成CO,反应的化学方程式是________;实验时,不需加热也能产生CO,其原因是_______。
(2)如需收集CO气体,连接上图中的装置,其连接顺序为:a→__________(按气流方向,用小写字母表示)。
Ⅱ.对一氧化碳的化学性质进行探究
资料:ⅰ.常温下,CO与PdCl2溶液反应,有金属Pd和CO2生成,可用于检验CO;
ⅱ.一定条件下,CO能与NaOH固体发生反应:CO+NaOH![]() HCOONa
HCOONa
利用下列装置进行实验,验证CO具有上述两个性质。
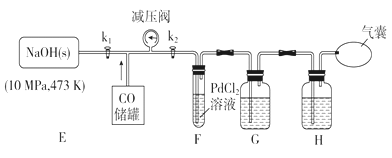
(3)打开k2,F装置中发生反应的化学方程式为_____________;为了使气囊收集到纯净的CO,以便循环使用,G装置中盛放的试剂可能是_________,H装置的作用是____________。
(4)现需验证E装置中CO与NaOH固体发生了反应,某同学设计下列验证方案:取少许固体产物,配置成溶液,在常温下测该溶液的pH,若pH>7,证明CO与NaOH固体发生了反应。该方案是否可行,请简述你的观点和理由:________,_________。
(5)25℃甲酸钠(HCOONa)的水解平衡常数Kh的数量级为____________。若向100ml 0.1mol.L-1的HCOONa溶液中加入100mL0.2mol.L-1的HCl溶液,则混合后溶液中所有离子浓度由大到小排序为_________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)在一定温度下,有下列反应发生:Fe2O3(s)+3CO(g) 2Fe(s)+3CO2(g),该反应的平衡常数表达式K=________。
(2)在配制FeCl3溶液时,加入少许浓盐酸,其目的是:_____________;不断加热FeCl3溶液,蒸干其水分并灼烧固体,最后得到的物质是________。
(3)已知:Fe2O3(s)+![]() C(s)=
C(s)=![]() CO2(g)+2Fe(s) ΔH=+234.1 kJ/mol
CO2(g)+2Fe(s) ΔH=+234.1 kJ/mol
C(s)+O2(g)===CO2(g) ΔH=-393.5 kJ/mol
则2Fe(s)+![]() O2(g)===Fe2O3(s)的ΔH是____________________。
O2(g)===Fe2O3(s)的ΔH是____________________。
(4)Fe(OH)2在空气中短时间内可被氧化为Fe(OH)3,发生的反应为:4Fe(OH)2+O2+2H2O=4Fe(OH)3,下列说法中错误的是________(填字母)。
A.该反应是能自发进行的反应
B.该反应是熵增加的反应
C.该反应是化合反应
D.该反应是氧化还原反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】用惰性电极电解一定浓度的硫酸铜溶液,通电一段时间后,向所得的溶液中加入0.1 mol Cu2(OH)2CO3后恰好恢复到电解前的状态(不考虑二氧化碳的溶解),则电解过程中共转移电子的物质的量为
A.0.4 molB.0.5 molC.0.6 molD.0.8 mol
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】根据反应路线及所给信息填空。

(1)烃A的结构简式是___________,名称是___________________。
(2)①的反应类型是:_____________。③的反应类型是:______________。
(3)反应④的化学方程式是_____________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】碳排放是影响气候变化的重要因素之一。最近,科学家开发出一种新系统,“溶解”水中的二氧化碳,以触发电化学反应,生成电能和氢气,其工作原理如图所示。下列有关说法中不正确的是( )
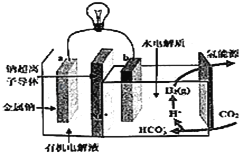
A. 系统工作时,化学能转变成电能
B. 系统工作时,电流由a极沿导线流向b极
C. 系统工作时,b极区可能会析出固体
D. 系统工作时,b极区的电极反应式为2CO2+2H2O+2e﹣=2HCO3﹣+H2
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com