
| A. | 漂白粉和二氧化氯 | B. | 二氧化硫和次氯酸 | ||
| C. | 二氧化硫和漂白粉 | D. | 活性炭和二氧化硫 |
分析 漂白粉、次氯酸漂白原理相同,都是因为具有强氧化性,能氧化有机色素而具有漂白性,二氧化硫能够与有机色素化合生成无色物质而具有漂白性,活性炭具有较大的表面积,具有吸附作用而具有漂白极性,据此解答.
解答 解:A.漂白粉和二氧化氯都是因为具有强氧化性而具有漂白性,漂白原理相同,故A选;
B.二氧化硫为化合漂白,次氯酸为氧化性漂白,二者漂白原理不同,故B不选;
C.二氧化硫为化合漂白,漂白粉为氧化性漂白,二者漂白原理不同,故C不选;
D.活性炭为吸附性漂白,二氧化硫为化合漂白,二者原理不同,故D不选;
故选:A.
点评 本题考查了具有漂白性物质的漂白原理的实质分析,主要考查次氯酸、二氧化硫、臭氧、活性炭的漂白原理,反应实质,较简单.


科目:高中化学 来源: 题型:解答题
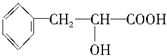
 (只要求写出一个化学方程式,有机物写结构简式).
(只要求写出一个化学方程式,有机物写结构简式).查看答案和解析>>
科目:高中化学 来源: 题型:推断题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
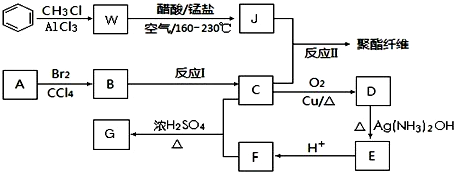
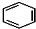 +RCl$\stackrel{AlCl_{3}}{→}$
+RCl$\stackrel{AlCl_{3}}{→}$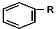 +HCl(-R为烃基)
+HCl(-R为烃基)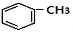 $→_{空气/160-230℃}^{醋酸/锰盐}$
$→_{空气/160-230℃}^{醋酸/锰盐}$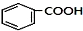
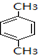 .
.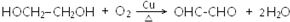 .
.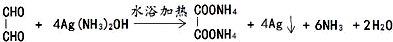 .
.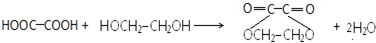 .
.查看答案和解析>>
科目:高中化学 来源: 题型:计算题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 苯与浓硫酸共热并保持70-80℃反应生成苯磺酸 | |
| B. | 苯乙烯在合适条件下催化加氢可生成乙基环己烷 | |
| C. | 乙烯与溴的四氯化碳溶液反应生成1,2-二溴乙烷 | |
| D. | 甲苯与氯气在光照下反应主要生成2,4-二氯甲苯 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 物质发生化学反应都伴随着能量变化 | |
| B. | 化学反应的速率和限度均可通过改变化学反应条件而改变 | |
| C. | 可逆反应只是代表少数反应 | |
| D. | 化学反应达到平衡状态时,正反应速率与逆反应速率相等 |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
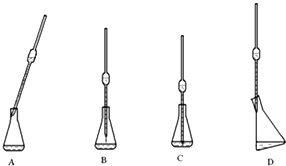 利用所学化学知识解答问题:
利用所学化学知识解答问题:查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 1:6 | B. | 6:1 | C. | 1:5 | D. | 5:1 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com