
| 要提纯的物质 (杂质) | 溴乙烷 (乙醇) | 乙醇 (水) | 乙醇 (乙酸) | 溴苯 (溴) |
| (1)选用试剂 | ||||
| (2)分离方法 |
分析 乙醇与水互溶,溴乙烷不溶于水;
CaO与水反应后,增大与乙醇的沸点差异;
乙酸与NaOH反应后,增大与乙醇的沸点差异;
溴与NaOH反应后,与溴苯分层.
解答 解:乙醇与水互溶,溴乙烷不溶于水,则选择试剂为水,分离方法为分液;
CaO与水反应后,增大与乙醇的沸点差异,则选择试剂为生石灰,分离方法为蒸馏;
乙酸与NaOH反应后,增大与乙醇的沸点差异,则选择试剂为氢氧化钠,分离方法为蒸馏;
溴与NaOH反应后,与溴苯分层,则选择试剂为氢氧化钠,分离方法为分液,
故答案为:
| 要提纯的物质 (杂质) | 溴乙烷 (乙醇) | 乙醇 (水) | 乙醇 (乙酸) | 溴苯 (溴) |
| (1)选用试剂 | e | c | b | b |
| (2)分离方法 | B | C | C | B |
点评 本题考查混合物分离提纯,为高频考点,把握物质的性质、发生的反应、混合物分离方法为解答的关键,侧重分析与应用能力的考查,注意有机物的性质应用,题目难度不大.


科目:高中化学 来源: 题型:选择题
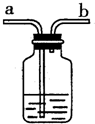
| A. | b导管连接供给氧气的钢瓶 | |
| B. | b导管连接病人吸氧气的塑料管 | |
| C. | 使用该装置用来观测是否有氧气输出 | |
| D. | 使用该装置用来观测氧气输出的速率 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
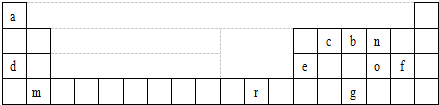
| A | B | ||||||
| D | E | F | |||||
| C | G | H |
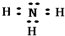 ;该物质溶于水后的溶液呈碱性(填“酸”、“碱”或“中”).
;该物质溶于水后的溶液呈碱性(填“酸”、“碱”或“中”).查看答案和解析>>
科目:高中化学 来源: 题型:解答题
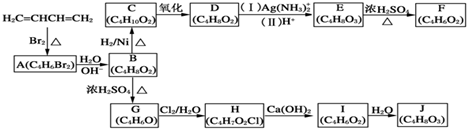
 +H2O,
+H2O,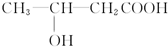 和
和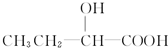 以外,还有
以外,还有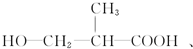 、
、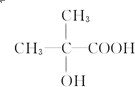 (写出结构简式,不考虑立体异构).
(写出结构简式,不考虑立体异构). ;
;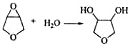 .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
 我国自行设计和生产的电动燃料汽车,该车装有“绿色心脏”--质子交换膜燃料电池,其工作原理如图所示.则下列叙述正确的( )
我国自行设计和生产的电动燃料汽车,该车装有“绿色心脏”--质子交换膜燃料电池,其工作原理如图所示.则下列叙述正确的( )| A. | 通入O2的电极发生氧化反应 | |
| B. | 通入H2的电极是正极 | |
| C. | 正极的电极反应为O2+4H++4e-═2H2O | |
| D. | 总反应的化学方程式为:O2+2H2$\frac{\underline{\;点燃\;}}{\;}$2H2O |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 ;
;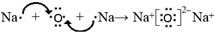 ;
;查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 在阴离子中,质子数一定少于核外电子数 | |
| B. | 氧化反应就是物质与氧气发生的反应 | |
| C. | 在化学反应中加入催化剂一定能加快反应的速率 | |
| D. | 最外层电子数为8的粒子一定是稀有气体元素的原子 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
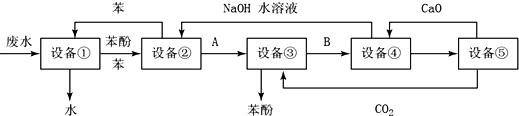
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com