
| ɫ̬ | ���ڼ� | ����1kPa���� ������ | |
| �������� | -59-11����ɫҺ�� | �����������κ������� | ��ը |
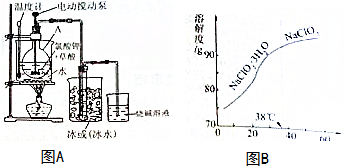
���� �ó�ʪ��KCIO3�Ͳ��ᣨH2C2O2����60��ʱ��Ӧ��ȡ�ռ�Һ̬ClO2��Ϊ�����¶Ⱥ㶨����Ӧ����ˮԡ���ȵ������½��У���Ӧװ���õ��綯����ý��裬��ʹ��Ӧ���ֽӴ�������Ӧ���ʣ�Ϊ��ֹClO2�ӷ���Ӧ�����ռ�����������������Һ����β�����գ�
����ͼ���������Ƶ��ܽ������ȷ�������ܽ�����߿��Կ�������ѹ���Ը���38��ʱ��������ĸҺ�е�NaClO2̫�ֻ࣬�м�ѹʱ������
�ɸ�������������������������⻯�ص�����Һ��Ӧ���۲���Һ�Ƿ����ɫ���������ԣ�
��� �⣺�ó�ʪ��KCIO3�Ͳ��ᣨH2C2O2����60��ʱ��Ӧ��ȡ�ռ�Һ̬ClO2��Ϊ�����¶Ⱥ㶨����Ӧ����ˮԡ���ȵ������½��У���Ӧװ���õ��綯����ý��裬��ʹ��Ӧ���ֽӴ�������Ӧ���ʣ�Ϊ��ֹClO2�ӷ���Ӧ�����ռ�����������������Һ����β�����գ�
��1����ʵ��װ��ͼ��֪AΪԲ����ƿ���ʴ�Ϊ��Բ����ƿ��
��2����Ӧ����60��ʱ���У���Ҫ�¶ȼƲ�����Ӧ�¶ȣ��Ա���Ʒ�Ӧ�¶ȣ���Ӧװ���õ��綯����ý��裬��ʹ��Ӧ���ֽӴ�������Ӧ���ʣ�
�ʴ�Ϊ��������Ӧ�¶ȣ�����Ӧ���ʣ�
��3����-59-11��Ϊ���ɫҺ�壬�ҳ���1kPa���Ȼ����ⱬը��Ӧ�ڵ����±ܹⱣ�棬�ʴ�Ϊ��d��
��4��Ϊ��ֹClO2��Ⱦ��������ClO2������������Һ��Ӧ�����������κ������Σ���������������Һ����β�����ʴ�Ϊ������β����
��5���ٴ��ܽ�����߿��Կ�������ѹ���Ը���38��ʱ��������ĸҺ�е�NaClO2̫�ֻ࣬�м�ѹʱ���������Ը���38��ʱˮ�ֻӷ���һЩ��ĸҺ��һЩ��
���ʴ�Ϊ����ѹ�������¶��Ը��ڣ�����ڣ�38�棻
���ڵ��۵⻯����Һ�м�������NaClO2��Һ��������������ϡ���ᣬ��Һ������˵�����ɵ⣬���˵���������Ƶ�������ǿ�ڵ⣮
�ʴ�Ϊ���ڵ��۵⻯����Һ�м�������NaClO2��Һ��������������ϡ���ᣬ��Һ����˵���������Ƶ�������ǿ�ڵ⣮
���� ���⿼�����Ʊ�ʵ�鷽����ơ���ѧʵ�鷽�����۵�֪ʶ�㣬��ȷʵ��ԭ���ǽⱾ��ؼ����Ӱ�ȫ�ԡ������ԡ��ɲ����Եȷ����ٽ�����ʵ����������ʵ�飬ʵ�����ͬʱ����ѧ��˼ά�������ԡ������������Եȣ���Ŀ�Ѷ��еȣ�


 һ����ʦȨ����ҵ��ϵ�д�
һ����ʦȨ����ҵ��ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
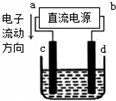
| A�� | a������b���� | B�� | a������b���� | ||
| C�� | �������У�������Ũ�Ȳ��� | D�� | �������У�d�缫������� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ��������ƽ��ȡ28.6g Na2CO3•10H2O���� | |
| B�� | ��Na2CO3�����������ƿ�У���ˮ���̶��� | |
| C�� | ����ʱ����Һ�棬������ҺŨ��ƫ�� | |
| D�� | ��ˮʱ���������̶��ߣ��ý�ͷ�ι�ֱ����������Һ�� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com