
| A. | Cu与硝酸 | B. | SO2与NaOH溶液 | C. | Na与O2 | D. | Fe与Cl2 |
分析 A、铜和浓硝酸以及稀硝酸反应生成的产物不同;
B、少量二氧化硫和烧碱反应生成亚硫酸钠,二氧化硫过量时生成亚硫酸氢钠;
C、Na与O2反应在不同条件下产物不同;钠在氧气中加热反应生成过氧化钠,在氧气中常温下反应生成氧化钠,产物不同;
D、铁和氯气反应只能将铁氧化为正三价.
解答 解:A、铜和浓硝酸反应生成二氧化氮,与稀硝酸反应生成一氧化氮,是浓度不同,而产物不同,故A错误;
B、少量二氧化硫和烧碱反应生成亚硫酸钠,二氧化硫过量时生成亚硫酸氢钠,因反应物用量不同而产物不同,故B正确;
C、钠在氧气中加热反应生成过氧化钠,在氧气中常温下反应生成氧化钠,条件不同而产物不同,故C错误;
D、铁和氯气反应只能将铁氧化为正三价,反应条件、用量、浓度等不同时所发生的化学反应相同,故D错误;
故选B.
点评 本题考查学生物质之间反应时,用量的多少,反应条件的不同,对反应产物会产生影响,可以根据所学知识来回答,难度中等.


 新课标同步训练系列答案
新课标同步训练系列答案 一线名师口算应用题天天练一本全系列答案
一线名师口算应用题天天练一本全系列答案 小学学习好帮手系列答案
小学学习好帮手系列答案科目:高中化学 来源: 题型:选择题
| A. | 萃取在香料、药物的提取应用广泛 | |
| B. | 用乙醇作萃取剂,萃取碘水中的碘单质 | |
| C. | 用四氯化碳萃取碘水时,下层溶液呈紫色 | |
| D. | 萃取后的混合物进行分离时,要使用分液漏斗 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 溶液 | 胶体 | 浊液 | |
| 光路示意图 |  |  |  |
| 对光的主要作用 | 透射 | 散射 | 反射或折射 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 氯气、二氧化硫都能使品红溶液褪色,它们的漂白原理相同 | |
| B. | 纯净的晶体硅是现代光学及光纤制品的基本原料 | |
| C. | 用丁达尔效应可鉴别FeCl3溶液和Fe(OH)3胶体 | |
| D. | NH3的水溶液可以导电,所以NH3是电解质 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
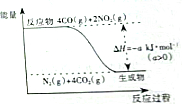 研究NOx、SO2、CO等大气污染气体的处理方法具有重要意义.
研究NOx、SO2、CO等大气污染气体的处理方法具有重要意义.查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com