
已知氨可以与灼热的氧化铜反应得到氮气和金属铜,用下图中的装置可以实现该反应。

请回答下列问题:
(1)A中加入的物质是________,发生反应的化学方程式是________________________________________________________________________。
(2)B中加入的物质是________,其作用是________________________________________________________________________________________________________________________________________________。
(3)实验时在C中观察到的现象是________________________________________________________________________,
发生反应的化学方程式是________________________________________________________________________。
(4)实验时在D中观察到的现象是________________________________________________________________________,
D中收集到的物质是_______,检验该物质的方法和现象是________________________________________________________________________。
解析 实验装置:气体发生装置→气体净化装置→氨气还原氧化铜装置→产物①收集装置→产物②收集装置。
(1)该装置属于“固(Ⅰ)+固(Ⅱ) 气”装置,实验室选择氯化铵固体与消石灰反应制氨气,发生的反应为2NH4Cl+Ca(OH)2
气”装置,实验室选择氯化铵固体与消石灰反应制氨气,发生的反应为2NH4Cl+Ca(OH)2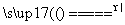 CaCl2+2NH3↑+2H2O。
CaCl2+2NH3↑+2H2O。
(2)装置中用U管干燥氨气,只能用固体干燥剂,干燥氨气须用碱石灰、生石灰、固体氢氧化钠等碱性干燥剂,不能用酸性干燥剂,也不能用氯化钙。
(3)根据实验目的可知,硬质试管C中的固体为氧化铜,发生反应:2NH3+3CuO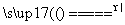 3Cu+N2+3H2O,实验现象是黑色粉末逐渐变成红色。
3Cu+N2+3H2O,实验现象是黑色粉末逐渐变成红色。
(4)反应生成的N2及水蒸气和未反应的NH3均会从C装置中进入D试管中,因为水蒸气在冰水的作用下转化为液态水,NH3极易溶于水,故D中收集到的是氨水。E装置收集到的是N2。
答案 (1)固体NH4Cl和Ca(OH)2 2NH4Cl+Ca(OH)2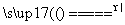 CaCl2+2NH3↑+2H2O(其他合理答案也可)
CaCl2+2NH3↑+2H2O(其他合理答案也可)
(2)碱石灰(或CaO) 除去氨气中的水蒸气
(3)黑色粉末逐渐变为红色 2NH3+3CuO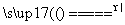 N2+3H2O+3Cu
N2+3H2O+3Cu


 一诺书业暑假作业快乐假期云南美术出版社系列答案
一诺书业暑假作业快乐假期云南美术出版社系列答案科目:高中化学 来源: 题型:
常温下测得某无色溶液中水电离出c(H+)=1×10-11mol/L,又知该溶液中还有大量NO3-、NH4+、Cl-,那么该溶液中还一定大量存在的离子是( )
A.[Al(OH)4]-、ClO- B.Mg2+、SO42-
C.Cu2+、HCO3- D.Ba2+、I-
查看答案和解析>>
科目:高中化学 来源: 题型:
下列离子方程式书写正确的是( )
A.澄清石灰水中通入过量的CO2:Ca2++2OH-+CO2===CaCO3↓+H2O
B.碳酸钠溶液中加入二氧化硅:CO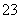 +SiO2===SiO
+SiO2===SiO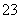 +CO2↑
+CO2↑
C.二氧化硅与烧碱溶液反应:SiO2+2OH-===SiO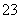 +H2O
+H2O
D.硅酸和烧碱溶液中和:H++OH-===H2O
查看答案和解析>>
科目:高中化学 来源: 题型:
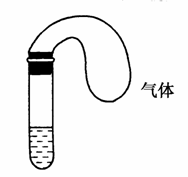
已知NH3溶于水得氨水,呈碱性。某学校课外活动小组利用右图所示装置分别做如下实验:
(1)在试管中注入某红色溶液,加热试管,溶液颜色逐渐变浅,冷却后恢复红色,则原溶液可能是________溶液;加热时溶液由红色逐渐变浅的原因是
________________________________________________________________________。
(2)在试管中注入某无色溶液,加热试管,溶液变为红色,冷却后恢复无色,则此溶液可能是________________________溶液;加热时溶液由无色变为红色的原因是______________________ __________________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
下列实验操作正确的是( )
A.当某实验没有明确的药品用量说明时,为看到明显现象,取用药品越多越好
B.取用细口瓶里的试液时,先拿下瓶塞,倒放在桌上,然后标签朝外拿起瓶子,瓶口要紧挨着试管口,使液体缓缓地倒入试管中
C.胶头滴管取完一种试液后,直接取用另一种不与其反应的试液
D.取用粉末状固体或固体颗粒时,应用药匙或纸槽,取用块状固体时,应用镊子夹取
查看答案和解析>>
科目:高中化学 来源: 题型:
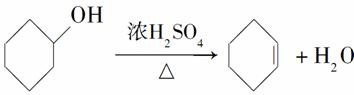
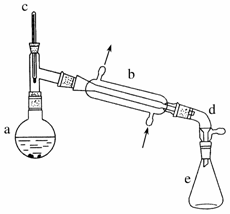
醇脱水是合成烯烃的常用方法,实验室合成环己烯的反应和实验装置如下:
可能用到的有关数据如下:
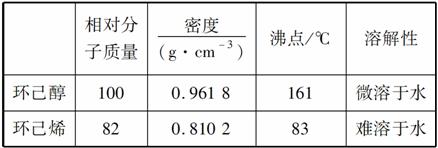
合成反应:
在a中加入20 g环己醇和2 小片碎瓷片,冷却搅动下慢慢加入1 mL,浓硫酸。b中通入冷却水后,开始缓慢加热a,控制馏出物的温度不超过90 ℃。
分离提纯:
反应粗产物倒入分液漏斗中分别用少量5%碳酸钠溶液和水洗涤,分离后加入无水氯化钙颗粒,静置一段时间后弃去氯化钙。最终通过蒸馏得到纯净环己烯10 g。
回答下列问题:
(1)装置b的名称是________。
(2)加入碎瓷片的作用是________;如果加热一段时间后发现忘记加瓷片,应该采取的正确操作是________(填正确答案标号)。
A.立即补加 B.冷却后补加
C.不需补加 D.重新配料
(3)本实验中最容易产生的副产物的结构简式为______________________。
(4)分液漏斗在使用前须清洗干净并________;在本实验分离过程中,产物应该从分液漏斗的____________(填“上口倒出”或“下口放出”)。
(5)分离提纯过程中加入无水氯化钙的目的是________________________________________________________________________。
(6)在环己烯粗产物蒸馏过程中,不可能用到的仪器有________(填正确答案标号)。
A.圆底烧瓶 B.温度计 C.吸滤瓶
D.球形冷凝管 E.接收器
(7)本实验所得到的环己烯产率是________ (填正确答案标号)。
A.41% B.50%
C.61% D.70%
查看答案和解析>>
科目:高中化学 来源: 题型:
下列实验现象及相关的离子方程式均正确的是
A.C12与FeI2溶液反应,当以n(C12)︰n(FeI2)=1︰1时:
2Fe2+ +2I- +2C12 =2Fe3+ +I2 +4Cl-
B.向Ba(NO3)2溶液中通入S02气体,出现白色沉淀:
Ba2+ +SO2 +H2O==BaSO3↓ +2H+
C.向H2O2 溶液中滴加酸化的KMnO4 溶液,KMnO4 溶液褪色:
2MnO4‾ +7H2O2 +6H+==2 Mn2+ +6O2 ↑+10H2O
D.将等物质的量浓度、等体积的Ba(OH)2溶液和NaHS04溶液混合:
Ba2++SO42‾+H++OH‾ ==BaSO4 ↓+H2O
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com