
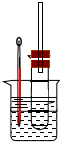
 溴乙烷在不同溶剂中与NaOH发生不同类型的反应,生成不同的反应产物.某同学依据溴乙烷的性质,用如图实验装置(铁架台、酒精灯略)验证
溴乙烷在不同溶剂中与NaOH发生不同类型的反应,生成不同的反应产物.某同学依据溴乙烷的性质,用如图实验装置(铁架台、酒精灯略)验证分析 (1)水浴加热,可提供稳定的加热温度,且避免溴乙烷的挥发;
(2)溴乙烷不溶于水,开始溶液分层,生成物乙醇、溴化钠都溶于水;
(3)溴乙烷与NaOH溶液发生水解反应生成乙醇和溴化钠;溴乙烷在NaOH乙醇溶液中发生消去反应,生成乙烯,乙烯能够使酸性的高锰酸钾褪色(或者使溴的四氯化碳褪色),只要证明乙烯的存在即可证明发生的是消去反应.
解答 解:(1)溴乙烷沸点低,溴乙烷易挥发,用水浴加热热均匀,减少溴乙烷的损失.
故答案为:溴乙烷沸点低,减少溴乙烷的损失;
(2)溴乙烷不溶于水,开始溶液分层,生成物乙醇、溴化钠都溶于水,当溶液分层消失,表明溴乙烷与NaOH溶液已完全反应.
故答案为:试管内溶液静置后不分层;
(3)溴乙烷与NaOH溶液发生水解反应生成乙醇和溴化钠,反应的方程式为CH3CH2Br+NaOH $→_{△}^{水}$CH3CH2OH+NaBr,溴乙烷在NaOH乙醇溶液中发生消去反应,生成乙烯,只有证明乙烯的存在即可证明发生的是消去反应,方法是:将生成的气体先通过盛有水的试管,再通入盛有酸性KMnO4溶液的试管,酸性KMnO4溶液褪色(或直接通入溴的四氯化碳溶液,四氯化碳褪色),
故答案为:CH3CH2Br+NaOH $→_{△}^{水}$CH3CH2OH+NaBr;生成的气体;将生成的气体先通过盛有水的试管,再通入盛有KMnO4溶液的试管,KMnO4溶液褪色(或直接通入溴的四氯化碳溶液).
点评 考查卤代烃的性质、反应原理的探究、对实验装置的理解等,难度不大,注意(2)中取代反应实质是,溴乙烷与是发生取代反应生成乙醇与氢溴酸,氢溴酸与氢氧化钠反应生成溴化钠与水,所以还发生中和反应.


科目:高中化学 来源: 题型:推断题
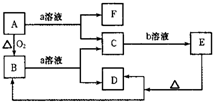 已知如图中A是固体单质,E是一种白色沉淀,F为密度最小的无色气体.且各种物质所含元素除H、O外,其余均为第三周期元素.
已知如图中A是固体单质,E是一种白色沉淀,F为密度最小的无色气体.且各种物质所含元素除H、O外,其余均为第三周期元素.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 反应过程中,若增大压强能提高SiCl4的转化率 | |
| B. | 若反应开始时SiCl4为1 mol,则达到平衡时,吸收热量为Q kJ | |
| C. | 反应至4 min时,若HCl浓度为0.12 mol•L-1,则H2的反应速率为0.03 mol•(L•min-1) | |
| D. | 当反应吸收热量为0.025Q kJ时,生成的HCl通入100 mL 1 mol•L-1的NaOH溶液中恰好反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

 两种有机物的结构简式
两种有机物的结构简式 ;
; .
.查看答案和解析>>
科目:高中化学 来源: 题型:实验题
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
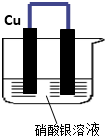 如图所示,将铁、铜通过导线相连,置于硝酸银溶液中.
如图所示,将铁、铜通过导线相连,置于硝酸银溶液中.查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com