
| A、原氨水的浓度=10-3mol/L | ||||
B、溶液中
| ||||
| C、氨水的电离程度增大,溶液中所有离子的浓度均减小 | ||||
| D、再加入10mL pH=3的盐酸充分反应后混合液的pH值肯定大于7 |
c( N
| ||
| c( NH3? H2 O) |


科目:高中化学 来源: 题型:
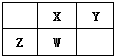 短周期元素X、Y、Z、W在元素周期表中的位置如图所示,其中X形成化合物种类最多,下列说法正确的是( )
短周期元素X、Y、Z、W在元素周期表中的位置如图所示,其中X形成化合物种类最多,下列说法正确的是( )| A、W位于第三周期IV族 |
| B、Y的气态氢化物的水溶液中只存在两个平衡状态 |
C、X的最高价氧化物的电子式是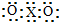 |
| D、常温下,将Z单质投入到Y的最高价氧化物对应的水化物的浓溶液中,无明显现象 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、将pH=4的盐酸稀释后,溶液中所有离子的浓度均降低 |
| B、0.10mol?L-1的氨水加水稀释后,溶液中c(NH4+)、c(OH-)变大 |
| C、常温下,向水中加入少量Na2CO3固体后,c(H+)会减小,但Kw不变 |
| D、若V1L pH=11的NaOH溶液与V2L pH=3的HA溶液混合后显中性,则V1≤V2 |
查看答案和解析>>
科目:高中化学 来源: 题型:
 如图的装置中,干燥烧瓶中盛满某种气体,烧杯和滴管内盛放某种溶液.挤压滴管的胶头,下列与实验事实不相符的是( )
如图的装置中,干燥烧瓶中盛满某种气体,烧杯和滴管内盛放某种溶液.挤压滴管的胶头,下列与实验事实不相符的是( )| A、若a为CO2,b为NaOH溶液,可出现无色喷泉 |
| B、若a为HCl,b为AgNO3溶液,可出现白色喷泉 |
| C、若a为CO2,b为NaHCO3溶液,可出现无色喷泉 |
| D、若a为NH3,b为水(预先滴入少量酚酞溶液),可出现红色喷泉 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、金刚石比石墨更稳定 |
| B、等质量的石墨和金刚石,石墨具有的能量比金刚石高 |
| C、石墨比金刚石更稳定 |
| D、金刚石和石墨不能相互转化 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、7.80g Na2O2与5.85g NaCl所含阴离子数相等 |
| B、15g甲醛(HCHO)和乙酸的混合物中氧原子数为0.5NA |
| C、一定条件下,1.4g N2与0.2mol H2混合充分反应,转移的电子数为0.3NA |
| D、常温下,2L pH=12的Na2CO3溶液中含有的OH-数目为0.02NA |
查看答案和解析>>
科目:高中化学 来源: 题型:
 根据物质结构与性质的关系,请回答下列问题:
根据物质结构与性质的关系,请回答下列问题:查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com