
����Ŀ������A,B,C,D,E,F���ֳ���������Ԫ�أ���֪��
��Ԫ�ص�ԭ��������A��B��C��D��E��F��������ԭ�Ӱ뾶��E��F��B��C��D��A˳�����μ�С��
��A��Eͬ���壬A������Ԫ����ԭ�Ӱ뾶��С��Ԫ�أ�B���γ���Ȼ���ڵ���Ӳ�ĵ��ʼ������Ŀ����ң�DԪ��ԭ�������������Ǵ�����������3����
��C��E��F���ߵ�����������ˮ��������Ϊ���������죬��������֮����ɷ�Ӧ���ɿ������κ�ˮ�����������о���DԪ�أ�
��C��F����Ԫ��ԭ������������֮�͵���A��D��E����Ԫ��ԭ������������֮�ͣ�
��1��F��Ԫ�����ڱ��е�λ��Ϊ �� A��D��Ԫ��ԭ���γ�1��1�ͻ�����ĵ���ʽΪ ��
��2��B��ij��ԭ�ӳ����ڿ���ʱ�ⶨһЩ������������ԭ�ӷ���Ϊ ��
��3��д����+������Һ�з�Ӧ�����ӷ��� ��
��4�����ʼ��Ҽ���ת������ǡ����ǡ���������ԭ��Ӧ��
��5��C������������Ӧ��ˮ�����E�ļ��⻯�ﷴӦ������һ���κ�һ�����壬д���÷�Ӧ�Ļ�ѧ����ʽ �� �÷�Ӧ�����������뻹ԭ���������֮��Ϊ ��
���𰸡�
��1���������ڢ�A�壻![]()
��2��146C
��3��Al��OH��3+OH��=AlO2��+2H2O
��4������
��5��HNO3+NaH=NaNO3+H2����1��1
���������⣺�ٶ�����Ԫ�ص�ԭ��������A��B��C��D��E��F��������ԭ�Ӱ뾶��E��F��B��C��D��A˳�����μ�С����A��Eͬ���壬A������Ԫ����ԭ�Ӱ뾶��С��Ԫ�أ���AΪHԪ�أ�����ԭ������������2����EΪNa��B���γ���Ȼ���ڵ���Ӳ�ĵ��ʼ������Ŀ����ң���BΪ̼Ԫ�أ���Ϊ���ʯ����Ϊʯī��DԪ��ԭ�������������Ǵ�����������3��������������������8��ԭ��ֻ����2�����Ӳ㣬����������Ϊ6����DΪOԪ�أ���C��E��F���ߵ�����������ˮ��������Ϊ���������죬��������֮����ɷ�Ӧ���ɿ������κ�ˮ�����������о���DԪ�أ�Ӧ������������ǿ�ᡢǿ��֮��ķ�Ӧ����CΪNԪ�ء�EΪNa��FΪAl����ΪHNO3 �� ��ΪNaOH����ΪAl��OH��3����N��Al����Ԫ��ԭ������������֮�͵���H��O��Na����Ԫ��ԭ������������֮�ͣ��������⣮
��1.��FΪAl����Ԫ�����ڱ��е�λ��Ϊ���������ڢ�A�壬A��D��Ԫ��ԭ���γ�1��1�ͻ�����ΪH2O2 �� ����ʽΪ�� ![]() �����Դ��ǣ��������ڢ�A�壻
�����Դ��ǣ��������ڢ�A�壻 ![]() ��
��
��2.��B��ij��ԭ�ӳ����ڿ���ʱ�ⶨһЩ������������ԭ�ӷ���Ϊ146C�����Դ��ǣ�146C;
��3.����+������Һ�з�Ӧ�����ӷ��̣�Al��OH��3+OH��=AlO2��+2H2O�����Դ��ǣ�Al��OH��3+OH��=AlO2��+2H2O��
��4.�����ʯ��ʯī֮����ת������������ԭ��Ӧ�����Դ��ǣ����ǣ�
��5.��C������������Ӧ��ˮ����ΪHNO3 �� E�ļ��⻯��NaH��Ӧ������һ���κ�һ�����壬��Ӧ����NaNO3��H2 �� �÷�Ӧ�Ļ�ѧ����ʽHNO3+NaH=NaNO3+H2����������ʱ�����������ǻ�ԭ���NaHΪ��ԭ��������Ϊ���������÷�Ӧ�����������뻹ԭ���������֮��Ϊ1��1��
���Դ��ǣ�HNO3+NaH=NaNO3+H2����1��1��


 ��1����Ԫ�¿�������ĩϵ�д�
��1����Ԫ�¿�������ĩϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����ܱ������У��ϳɰ��ķ�ӦN2+3H2![]() 2NH3���ֽ�2mol N2��2mol H2ͨ��������з�Ӧ��20s������0.8 mol��NH3����H2��ת�����Ƕ��٣� ��
2NH3���ֽ�2mol N2��2mol H2ͨ��������з�Ӧ��20s������0.8 mol��NH3����H2��ת�����Ƕ��٣� ��
A. 70% B. 60% C. 50% D. 40%
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ȡ7.90gKMnO4�����ȷֽ��ʣ�����7.42g����ʣ�������������Ũ�����ڼ��������³�ַ�Ӧ�����ɵ�������A����������Ԫ����Mn2+���ڡ�
����㣺
��1��KMnO4�ķֽ���_______________��
��2������A�����ʵ���_____________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����������ڳ�����������ˮ���ܷ���ˮ�ⷴӦ����
A.����B.����C.������D.��������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��Ǧ���صĹ���ԭ��Ϊ��Pb+PbO2+2H2SO4�T2PbSO4+2H2O���ж�ͼ�������жϲ���ȷ����
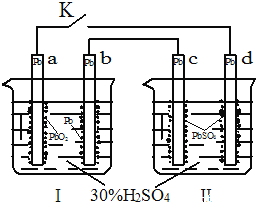
A. K�պ�ʱ��d�缫��Ӧʽ��PbSO4+2H2O-2e-�TPbO2+4H++SO42-
B. ����·��ת��0.2mol����ʱ��I�����ĵ�H2SO4Ϊ0.2mol
C. K�պ�ʱ��II��SO42-��c�缫Ǩ��
D. K�պ�һ��ʱ���II�ɵ�����Ϊԭ��أ�d�缫Ϊ����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������̿�ɴ���������Ⱦ��NO����Ӧԭ����C(s)��2NO(g)![]() N2(g)��CO2(g)��T ��ʱ����2 L�ܱ������м���0.100 mol NO��2.030 mol����̿(������)��ƽ��ʱ����̿���ʵ�����2.000 mol������˵������������(����)
N2(g)��CO2(g)��T ��ʱ����2 L�ܱ������м���0.100 mol NO��2.030 mol����̿(������)��ƽ��ʱ����̿���ʵ�����2.000 mol������˵������������(����)
A. ���¶��µ�ƽ�ⳣ����K��![]() B. �ﵽƽ��ʱ��NO��ת������60%
B. �ﵽƽ��ʱ��NO��ת������60%
C. 3 minĩ�ﵽƽ�⣬��v(NO)��0.01 mol��L��1��min��1 D. �����¶������ڻ���̿�����������Ⱦ��NO
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������ʵ�鷽����ʵ��������ȷ����(����)
A. ��pH��ֱֽ�ӷ���ij��Һ�У��ⶨ����Һ��pH
B. �ó���ʯ��ˮ����NaHCO3 ��Na2CO3
C. ���˲���ʱ��©���²��ļ���Ҫ�����ձ����ڱ�
D. �ӵ�ˮ��ȡ������Ҵ�����ȡ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�������йؽ����Ĺ�ҵ�Ʒ��У���ȷ���ǣ� ��
A.��������������Ϊԭ�ϻ���������ٵõ��Ȼ������壬������ڵ��Ȼ����õ���
B.��þ���ú�ˮΪԭ�ϣ���һϵ�й����Ƶ�����þ���壬�����������þ��þ
C.���ƣ��ú�ˮΪԭ���Ƶþ��Σ��ٵ�ⴿ����NaCl��Һ
D.������������ʯΪԭ�ϣ����ý�̿��������Ӧ���ɵ�CO�ڸ����»�ԭ����
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com