
【题目】I.氟及其化合物用途非常广泛。回答下列问题:
(1)聚四氟乙烯商品名称为“特氟龙”,可做不粘锅涂层。它是一种准晶体,该晶体是一种无平移周期序、但有严格准周期位置序的独特晶体。可通过____________方法区分晶体、准晶体和非晶体。
(2)锑(Sb)与砷处于同一主族且相邻,基态锑原子价电子排布式为______。[H2F]+[SbF6]-(氟酸锑)是一种超强酸,存在[H2F]+,写出一种与[H2F]+互为等电子体的阴离子是_________。
(3)硼酸(H3BO3)和四氟硼酸铵(NH4BF4)都有着重要的化工用途。
①H3BO3和NH4BF4涉及的四种元素中第二周期元素的第一电离能由大到小的顺序____(填元素符号)。
②H3BO3本身不能电离出H+,在水中易结合一个OH﹣生成[B(OH)4]﹣,而体现弱酸性。[B(OH)4]﹣中B原子的杂化类型为_________。
③NH4BF4(四氟硼酸铵)可用作铝或铜焊接助熔剂、能腐蚀玻璃等。四氟硼酸铵中存在_______(填序号):
A 离子键 B σ键 C π键 D 范德华力 E 配位键
(4)CuCl的熔点为426℃,熔化时几乎不导电;CuF的熔点为908℃。
①CuF比CuCl熔点高的原因是_____________;
②CuF的晶胞结构如图1。F-填充在Cu+围成的_______空隙中,空隙填充率为________%。
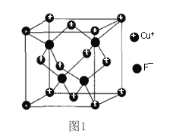
Ⅱ.AA705合金(含Cu、Al、Zn、Mg和Ti)几乎与钢一样坚固,但重量仅为钢的三分之一,已被用于飞机机身和机翼、智能手机外壳上等。
(5)CN-、NH3、H2O和OH-等配体都能与Zn2+形成配离子。1mol [Zn(NH3)4]2+含________ molσ键,中心离子的配位数为__________。
钛晶体有两种品胞,如图所示。
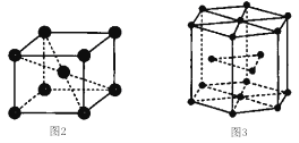
①如图2所示,晶胞的空间利用率为______(用含п的式子表示)。
②已知图3中六棱柱边长为x pm,高为y pm。该钛晶胞密度为D g·cm-3,NA为______mol-1(用含x y和D的式子表示)。
【答案】X—射线衍射 5s25p3 ![]() F>N>O>B sp3 ABE 由两者的熔点可知,CuCl是分子晶体,而CuF为离子晶体,离子晶体的熔点高 正四面体 50 16 4
F>N>O>B sp3 ABE 由两者的熔点可知,CuCl是分子晶体,而CuF为离子晶体,离子晶体的熔点高 正四面体 50 16 4 ![]()
![]() ×1030
×1030
【解析】
根据原子核外电子排布规律书写价电子排布式,根据等电子体原理书写等电子体,利用原子半径及全、半充满比较第一电离能大小,根据杂化轨道及价电子互斥理论判断杂化类型,根据配合物结构判断粒子间的作用力,根据晶胞结构结合均摊法和立体几何知识进行晶胞的相关计算。
Ⅰ.(1)从外观无法区分三者,区分晶体、非晶体、准晶体最可靠的方法是X—射线衍射法;
(2)锑为51号元素,Sb位于第五周期VA族,则基态锑(Sb)原子价电子排布式为5s25p3,[H2F]+[SbF6]-(氟酸锑)是一种超强酸,存在[H2F]+,[H2F]+中中心原子F的价层电子对数为2+![]() =4,σ键电子对数为2,该离子的空间构型为V型,与[H2F]+具有相同空间构型和键合形式的阴离子(即等电子体)为
=4,σ键电子对数为2,该离子的空间构型为V型,与[H2F]+具有相同空间构型和键合形式的阴离子(即等电子体)为![]() ;
;
(3)①H3BO3和NH4BF4涉及的四种元素中第二周期元素是B、N、O、F四种元素,同周期元素从左向右第一电离能呈增大趋势,N的2p能级半充满较稳定,N的第一电离能大于O,则这四种元素第一电离能由大到小的顺序为F>N>O>B;
②[B(OH)4]﹣中B的价层电子对=![]() ,所以B采取sp3杂化;
,所以B采取sp3杂化;
③NH4BF4(四氟硼酸铵)中含铵根离子和氟硼酸根离子,铵根离子中含3个σ键和1个配位键,氟硼酸根离子中含3个σ键和1个配位键,铵根离子和氟硼酸根离子以离子键相结合,则四氟硼酸铵中存在离子键、σ键、配位键,答案选ABE;
(4)①CuCl的熔点为426℃,熔化时几乎不导电,CuCl是分子晶体,而CuF的熔点为908℃,CuF为离子晶体,CuF离子晶体的晶格能大于CuCl分子间范德华力,故CuF比CuCl熔点高;
②根据CuF的晶胞结构图可知,F-填充在Cu+围成的正四面体空隙中,一个晶胞中存在8个正四面体空隙,其中4个被F-填充,故空隙填充率为50%;
Ⅱ.(5)所有单键包括配位键均为σ键,双键中有一个为σ键,每个NH3分子中含有3个N-H键,中心原子Zn与四个N原子之间存在配位键,则1mol [Zn(NH3)4]2+含(4+3×4)mol=16mol σ键,配位体为NH3,中心离子Zn2+的配位数为4;
①由图3可知,晶胞中钛原子的数目为1+8×![]() =2,设原子半径为r,则晶胞的对角线为4r,晶胞的边长为
=2,设原子半径为r,则晶胞的对角线为4r,晶胞的边长为![]() ,则空间利用率为
,则空间利用率为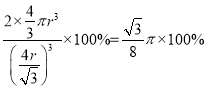 ;
;
②②图4晶胞中钛原子的数目为3+2×![]() +12×
+12×![]() =6,晶胞的质量为
=6,晶胞的质量为![]() g,六棱柱边长为x pm,高为y pm,则晶胞的体积为
g,六棱柱边长为x pm,高为y pm,则晶胞的体积为![]() x2y×10-30cm3,则D=
x2y×10-30cm3,则D=![]() g÷(
g÷(![]() x2y×10-30)cm3,由此计算得NA=
x2y×10-30)cm3,由此计算得NA=![]() mol-1。
mol-1。


 培优三好生系列答案
培优三好生系列答案 优化作业上海科技文献出版社系列答案
优化作业上海科技文献出版社系列答案科目:高中化学 来源: 题型:
【题目】(NH4)2Fe(SO4)2·6H2O俗称摩尔盐(M=392g·mol-1)是分析化学中重要的标准物质,某研究小组拟采用硫铁矿焙烧后的烧渣(主要成分为Fe2O3、SiO2、Al2O3,不考虑其他杂质)为原料制取摩尔盐,设计了如下流程:
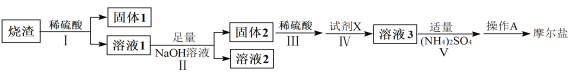
(1)写出试剂X的化学式__________。
(2)写出“溶液1”中某种离子与NaOH反应生成“溶液2”中离子的离子方程式________。
(3)操作A为蒸发浓缩至_________、冷却结晶、过滤、洗涤、干燥。其中过滤操作可用如图装置进行,请选择合适的编号,按正确的操作顺序补充完整(洗涤操作只需考虑一次):开抽气泵→a→b→d→_________→d→c→关抽气泵。
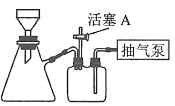
a.转移固液混合物
b.关活塞A
c.开活塞A
d.确认抽干
e.加洗涤剂洗涤
(4)实验制得的摩尔盐的纯度可用Ce(SO4)2标准溶液滴定进行测定。滴定反应为Fe2++Ce4+=Fe3++Ce3+。测定时,先称取4.000g样品,配成100mL溶液,取出其中20.00mL放入锥形瓶中,对溶液进行必要处理后,用0.1000mol·L-1Ce(SO4)2标准溶液滴定至终点,记录数据如下表:
滴定次数 | 0.1000mol·L-1Ce(SO4)2标准溶液体积(mL) | |
滴定前读数 | 滴定后读数 | |
1 | 0.10 | 20.12 |
2 | 0.12 | 20.10 |
3 | 0.05 | 21.65 |
①产品中摩尔盐的纯度为__________(用质量分数表示,保留4位有效数字)。
②若滴定过程中没有润洗滴定管,则会造成样品纯度______(填“偏高”、“偏低”或“无影响”)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】300多年前,著名化学家波义耳发现了铁盐与没食子酸的显色反应,并由此发明了蓝黑墨水。没食子酸的结构式如图所示:
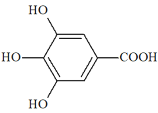
(1)1mol没食子酸与足量NaHCO3溶液反应,标准状况下可得________LCO2。
(2)没食子酸正丙酯具有抗氧化作用,是目前广泛应用的食品添加剂,其结构简式为______________.
(3)尼泊金酯是对羟基苯甲酸与醇形成的酯类化合物,是国家允许使用的食品添加剂。尼泊金丁酯的分子式为__________,其苯环只与—OH和—COOR两类取代基直接相连且两个取代基位于苯环对位的同分异构体有______种。
(4)写出尼泊金乙酯与氢氧化钠溶液加热反应的化学方程式:_____________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】硝酸铈铵、磷酸锰铵是两种重要的复盐,在工农业生产中具有广泛应用。
(1)复盐是由两种或两种以上金属离子(或铵根离子)和一种酸根离子构成的盐。下列物质属于复盐的是________(填序号)。
A.BaFe2O4 B.NaHSO4 C.KAl(SO4)2·12H2O D.Ag (NH3)2OH
(2)硝酸铈铵[(NH4)2Ce(NO3)6]的制备方法如下:
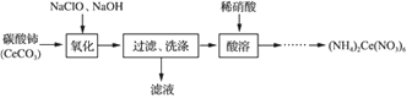
①“氧化”得到CeO2的化学方程式为______________。
②洗涤CeO2的方法是_____________。
(3)为测定磷酸锰铵[(NH4)aMnb(PO4)c·xH2O]的组成,进行如下实验:
①称取样品2.4480g,加水溶解后配成100.00mL溶液A;
②量取25.00mL溶液A,加足量NaOH溶液并充分加热,生成NH30.06720L(标准状况);
③另取25.00mL溶液A,边鼓空气边缓慢滴加氨水,控制溶液pH6~8,充分反应后,将溶液中Mn2+转化为Mn3O4,得Mn3O40.2290g。通过计算确定该样品的化学式(写出计算过程) __________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知![]() 、
、![]() 、
、![]() (z)互为同分异构体,下列说法不正确的是( )
(z)互为同分异构体,下列说法不正确的是( )
A.z的二氯代物有3种
B.x、y的一氯代物均只有3种
C.x、y因与Br2发生加成反应而使溴的四氯化碳溶液褪色
D.x、y、z中只有x的所有原子可能处于同一平面
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列有关物质的组成、结构和性质的说法中正确的是
A.用甘氨酸(![]() )和丙氨酸(
)和丙氨酸(![]() )缩合最多可形成四种二肽
)缩合最多可形成四种二肽
B.浓硫酸可以使蛋白质变黄,称为颜色反应,常用来鉴别部分蛋白质
C.在一定条件下,CH3CO18OH和C2H5OH反应可生成 CH3CO18OC2H5
D.HCOOH与OHCCH2OH属于同系物,均能使酸性KMnO4溶液褪色
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】艾司洛尔(Esmolol)是一种用于心房颤动、窦性心动过速以及手术期高血压的药物,其合成路线如下(部分条件已省略):
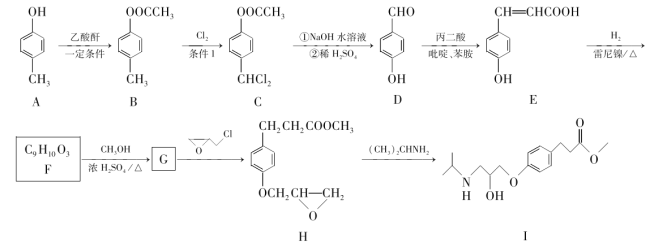
回答下列问题:
(1)A的化学名称是______。
(2)B→C的反应类型是______,条件1是______。
(3)D→E的反应中,除生成E外,还生成CO2,H2O,该反应的化学方程式为____________。
(4)F的结构简式为______。
(5)X为B的同分异构体,且为含羧基的芳香化合物,则X的结构有______种(不考虑立体异构),其中核磁共振氢谱有四组峰的同分异构体的结构简式为__________________(写一种)。
(6)肉桂酸(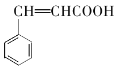 )是一种重要的食品添加剂、香料和医药中间体。以甲苯、丙二酸为起始原料制备肉桂酸的合成路线为____________________________________(其他试剂任选)。
)是一种重要的食品添加剂、香料和医药中间体。以甲苯、丙二酸为起始原料制备肉桂酸的合成路线为____________________________________(其他试剂任选)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列离子方程式正确的是
A.硫酸铝溶液中加入过量氨水:Al3++4OH-=AlO![]() +2H2O
+2H2O
B.二氧化硫与酸性高锰酸钾溶液反应:5SO2+2H2O+2MnO![]() =2Mn2++5SO
=2Mn2++5SO![]() +4H+
+4H+
C.Na2S2O3溶液与稀H2SO4反应的离子方程式:S2O![]() +6H+=2S↓+3H2O
+6H+=2S↓+3H2O
D.硫酸铜溶液中加少量的铁粉:3Cu2++2Fe=2Fe3++3Cu
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】DL—m—络氨酸是一种营养增补剂,能提高人体的免疫力。一种合成DL—m一络氨酸的路线如下:
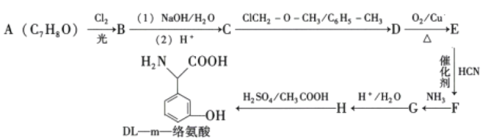
已知:①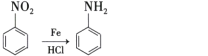
②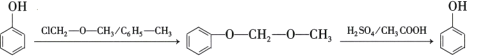
③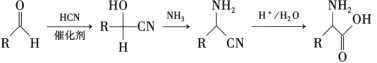
回答下列问题:
(1)A的化学名称为 ________,F中含氧官能团的名称是________。
(2)E到F的反应类型为________。
(3)写出D到E的化学方程式________。
(4)化合物M是一种α-氨基酸,是H的同分异构体。满足以下条件的M的同分异构体有________种。
i.环上有两个处于邻位上的取代基,与FeCl3溶液不能发生显色反应;
ii.1molM与足量金属钠反应产生1.5molH2。
其中分子中存在两个手性碳原子,且能在浓硫酸催化加热条件下发生消去反应而消除旋光性,该异构体的结构简式为________、________(已知:分子中存在手性碳原子的分子叫手性分子,手性分子具有旋光性)。
(5)![]() 是合成药物扑热息疼的中间体。设计由苯酚和ClCH2—O—CH3制备
是合成药物扑热息疼的中间体。设计由苯酚和ClCH2—O—CH3制备![]() 的合成路线________(无机试剂任选。)
的合成路线________(无机试剂任选。)
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com