
合成氨技术的创立开辟了人工固氮的重要途径,其研究来自正确的理论指导,合成氨反应的平衡常数K值和温度的关系如下:
| 温 度(℃) | 360 | 440 | 520 |
| K值 | 0.036 | 0.010 | 0.0038 |
 CO(g)+3H2(g) 获取,已知该反应中,当初始混合气
CO(g)+3H2(g) 获取,已知该反应中,当初始混合气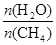 恒定时,温度、压强对平衡混合气CH4含量的影响如下图所示:
恒定时,温度、压强对平衡混合气CH4含量的影响如下图所示: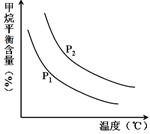
 CO2 (g)+H2(g) 获取。
CO2 (g)+H2(g) 获取。(1)①N2+3H2  2 NH3(2分)
2 NH3(2分)
② 随温度升高,反应的平衡常数K减小(2分) ③ a、d(2分)
(2)① <(1分) ②吸热(1分) (3)① 60 %(2分); 或2.25(2分) ② c和d(2分)
或2.25(2分) ② c和d(2分)
解析试题分析:(1)①工业上合成氨的原料是氮气和氢气,在一定温度、压强和催化剂作用下生成氨气,反应的化学方程式为N2+3H2  2 NH3。
2 NH3。
②根据表中数据可知,随着温度的升高,平衡常数K减小。这说明升高温度平衡向逆反应方向移动,因此正方应是放热反应。
③根据方程式可知,该反应是体积减小的、放热的可逆反应。a、增大压强,平衡向正反应方向移动,氢气的转化率增大,a正确;b、催化剂只能改变反应速率,而不能改变平衡状态,因此使用合适的催化剂不能提高氢气的转化率,b不正确;c、正方应是放热反应,升高温度平衡向逆反应方向移动 ,氢气的转化率降低,c不正确;d、及时分离出产物中的NH3,降低生成物氨气的浓度,平衡向正反应方向移动,氢气的转化率增大,d正确,答案选ad。
(2)①根据反应 CH4(g)+H2O (g) CO(g)+3H2(g) 可知,该反应是体积增大的可逆反应,因此增大越强,平衡向逆反应方向移动,甲烷的含量增大。所以根据图像可知,在温度相同的条件下,p1表示的甲烷含量低,这说明越强是P1小于P2。
CO(g)+3H2(g) 可知,该反应是体积增大的可逆反应,因此增大越强,平衡向逆反应方向移动,甲烷的含量增大。所以根据图像可知,在温度相同的条件下,p1表示的甲烷含量低,这说明越强是P1小于P2。
②根据图像可知,在越强相同的条件下,随着温度的升高,甲烷的含量降低。这说明升高温度平衡向正反应方向移动,因此该反应为吸热反应。
(3)① CO(g)+H2O(g) CO2 (g)+H2(g)
CO2 (g)+H2(g)
起始浓度(mol/L) 0.2 0.2 0 0
转化浓度(mol/L) 0.12 0.12 0.12 0.12
平衡浓度(mol/L) 0.08 0.08 0.12 0.12
所以平衡时CO的转化率=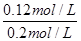 ×100%=60%
×100%=60%
化学平衡常数是在一定条件下,当可逆反应达到平衡状态时,生成物浓度的幂之积和反应物浓度的幂之积的比值,所以该温度下反应的平衡常数K= =
=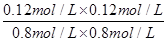 =
= 。
。
②在一定条件下,当可逆反应的正反应速率和逆反应速率相等时(但不为0),反应体系中各种物质的浓度或含量不再发生变化的状态,称为化学平衡状态,据此可以判断。a、反应前后体积不变,因此越强始终是不变的,则容器内压强不随时间改变不能说明反应达到平衡状态,a不正确;b、密度是混合气的质量和容器容积的比值,在反应过程中质量和容积始终是不变的,即密度始终是不变的,所以混合气体的密度不随时间改变不能说明反应达到平衡状态,b不正确;c、单位时间内生成a mol CO2的同时消耗a mol H2,由于单位时间内生成a mol CO2的同时还生成amol氢气,这说明正逆反应速率相等,可以说明达到平衡状态,c正确;d、由于反应前后体积不变,则可以用物质的量代替浓度,即如果混合气中n (CO) : n (H2O) : n (CO2) : n (H2)=1 : 16 : 6 : 6,则此时 =
=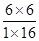 =
= ,因此恰好是平衡状态,d正确,答案选cd。
,因此恰好是平衡状态,d正确,答案选cd。
考点:考查合成氨原理;外界条件对平衡状态的影响;反应速率和平衡常数的计算、平衡状态的判断以及图像分析与应用等


 53随堂测系列答案
53随堂测系列答案科目:高中化学 来源: 题型:填空题
在一定体积的密闭容器中,进行如下化学反应:
Fe2O3(s)+3CO(g)  2Fe(s)+3CO2(g),其化学平衡常数K和温度t的关系如下表:
2Fe(s)+3CO2(g),其化学平衡常数K和温度t的关系如下表:
| t℃ | 1000 | 1150 | 1300 |
| K | 64.0 | 50.7 | 42.9 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
对于A(g)+B(g)  xC(g) ΔH 有:
xC(g) ΔH 有: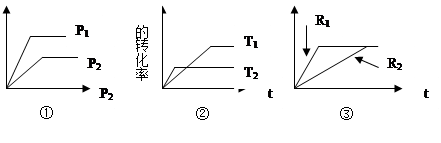
(1)①图表明P1 P2 ,且x的值为 ;
(2)②图表明T1 T2 ,且ΔH 0;
(3)如果③图R1,R2分别表示改变压强,则R1 R2 ,x的值为 ;
(4)如果③图分别表示有无催化剂,则R1表示 催化剂。
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
(6分)已知:T℃、P kpa时,容积为V 的密闭容器中充有1molA和2molB,保持恒温恒压使反应达平衡:A(g)+B(g) C(g),平衡时C 的体积分数为40℅。
C(g),平衡时C 的体积分数为40℅。
(1)欲保持温度、压强在上述条件下不变,在密闭容器中充入2molA和4molB,则平衡时体系容积为 ,C的体积分数为 。
(2)另取一个容积固定不变的密闭容器,仍控制温度为T℃,加入1molB和1molC,要使平衡时C 的体积分数仍为40℅,则该密闭容器体积为 。
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
在2L密闭容器内,800℃时反应:2NO(g)+O2(g)  2NO2(g)体系中,n(NO)随时间的变化如表:
2NO2(g)体系中,n(NO)随时间的变化如表:
| 时间(s) | 0 | 1 | 2 | 3 | 4 | 5 |
| n(NO)(mol) | 0.020 | 0.010 | 0.008 | 0.007 | 0.007 | 0.007 |
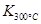 >
>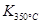 ,则该反应是 热反应。
,则该反应是 热反应。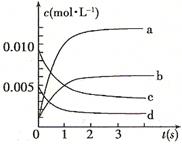
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
煤化工中常需研究不同温度下平衡常数、投料比及热值等问题。已知:
CO(g)+H2O(g) H2(g)+CO2(g)平衡常数随温度的变化如下表:
H2(g)+CO2(g)平衡常数随温度的变化如下表:
| 温度/℃ | 400 | 500 | 800 |
| 平衡常数K | 9.94 | 9 | 1 |
 H2(g)+CO2(g),当反应达平衡时,CO的体积分数为X,若维持容器的体积和温度不变,起始物质按下列四种配比充入该容器中,达到平衡时CO的体积分数不等于X的有
H2(g)+CO2(g),当反应达平衡时,CO的体积分数为X,若维持容器的体积和温度不变,起始物质按下列四种配比充入该容器中,达到平衡时CO的体积分数不等于X的有 查看答案和解析>>
科目:高中化学 来源: 题型:填空题
在一定体积的密闭容器中,进行如下反应:A(g) B(g)+C(g),其化学平衡常数K和温度t的关系如下表所示:
| toC | 700 | 800 | 830 | 1000 | 1200 |
| K | 0.6 | 0.9 | 1.0 | 1.7 | 2.6 |

| 时间t/min | 0 | 1 | 2 | 4 | 8 | 16 | 20 |
| C(A)/(mol·L-1) | 10.4 | 8.6 | 7.5 | 6.6 | 5.9 | 5.5 | 5.5 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
如图是煤化工产业链的一部分,试运用所学知识,解决下列问题:
(1)已知该产业链中某反应的平衡常数表达式为: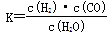 ,它所对应反应的化学方程式是
,它所对应反应的化学方程式是
_________________________________。
(2)合成甲醇的主要反应是:2H2(g)+CO(g) CH3OH(g)+90.8kJ,t℃下此反应的平衡常数为160。此温度下,在密闭容器中开始只加入CO、H2,反应l0min后测得各组分的浓度如下:
CH3OH(g)+90.8kJ,t℃下此反应的平衡常数为160。此温度下,在密闭容器中开始只加入CO、H2,反应l0min后测得各组分的浓度如下:
| 物质 | H2 | CO | CH3OH |
| 浓度(mol/L) | 0.2 | 0.1 | 0.4 |
| 反应 | 大气固氮 | 工业固氮 | ||||
| 温度/℃ | 27 | 2000 | 25 | 350 | 400 | 450 |
| K | 3.84×10-31 | 0.1 | 5×108 | 1.847 | 0.507 | 0.152 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
在一体积为10 L的容器中,通过一定量的CO和H2O,850 ℃时发生反应:
CO(g)+H2O(g)  CO2(g)+H2(g)
CO2(g)+H2(g)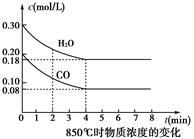
(1)CO和H2O浓度变化如图,则0~4 min的平均反应速率v(CO)=______mol·L-1·min-1。
(2)如图中4~5min之间该反应________(填“是”或“否”)处于平衡状态,判断理由________________________________________________________________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com