
分析 (1)根据n=cV计算HCl物质的量,再根据方程式Ba(OH)2+2HCl═BaCl2+2H2O计算Ba(OH)2的物质的量;
(2)试样加热后,固体质量减少为结晶水的质量,根据n=$\frac{m}{M}$计算结晶水的物质的量,结合(1)中3.50g试样含有Ba(OH)2的物质的量计算5.25g试样含有Ba(OH)2的物质的量,利用Ba(OH)2的物质的量与结晶水的物质的量关系计算n的值;
(3)根据m=nM计算3.5g试样中Ba(OH)2•nH2O的质量,进而计算试样中Ba(OH)2•nH2O的质量分数.
解答 解:(1)20.0mL 1.00mol/L 盐酸溶液中HCl的物质的量为0.02mol×1.00mol/L=0.02mol,
设溶液中氢氧化钡的物质的量为x,则:
Ba(OH)2+2HCl═BaCl2+2H2O,
1mol 2mol
x 0.02mol
故x=0.01mol
则3.50g试样含有Ba(OH)2的物质的量为0.01mol,
答:3.50g试样含有Ba(OH)2的物质的量为0.001mol;
(2)5.25g试样中含有Ba(OH)2的物质的量为0.01mol×$\frac{5.25g}{3.5g}$=0.015mol,含有水的物质的量为$\frac{5.25g-3.09g}{18g/mol}$=0.12mol,所以1:n=0.015mol:0.12mol,解得n=8,
答:Ba(OH)2•nH2O中的n值是8;
(3)3.50g试样含有Ba(OH)2的物质的量为0.01mol,即样品中Ba(OH)2•8H2O的物质的量为0.01mol,质量为0.01mol×315g/mol=3.15g,所以3.50g试样中Ba(OH)2•nH2O的质量分数为$\frac{3.15g}{3.5g}$×100%=90.0%,
故:试样中Ba(OH)2•nH2O的质量分数为90.0%.
点评 本题考查根据方程式的有关计算,侧重考查学生分析计算能力,难度不大.


科目:高中化学 来源: 题型:填空题
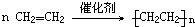 ;苯酚是医院常用的消毒剂,由于其有强烈的腐蚀作用,能腐蚀皮肤、气管,能使蛋白质变性,所以必须小心使用.中学化学常用浓溴水检验苯酚,请写出该反应的化学方程式
;苯酚是医院常用的消毒剂,由于其有强烈的腐蚀作用,能腐蚀皮肤、气管,能使蛋白质变性,所以必须小心使用.中学化学常用浓溴水检验苯酚,请写出该反应的化学方程式 ;
;查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | Mg2+、OH-、NO3-、K+ | B. | H+、HCO3-、Ca2+、NO3- | ||
| C. | Cl-、OH-、H+、K+ | D. | Cu2+、SO42-、Na+、Cl- |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 碳酸钠(固体) | B. | 水 | C. | 硫酸钾溶液 | D. | CH3COONa(固体) |
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | 单位物质的量的气体所占的体积就是气体摩尔体积 | |
| B. | 通常状况(室温、101kP)下,气体摩尔体积约为22.4 L/mol | |
| C. | 标准状况(0℃、101kP)下,气体摩尔体积约为22.4 L/mol | |
| D. | 标准状况(0℃、101kP)下,1 mol H2O的体积是22.4 L |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
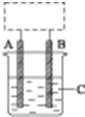 某学生设计了如图所示的装置(框内部分未画出),在装置内起初发生的反应为Cu+H2SO4═
某学生设计了如图所示的装置(框内部分未画出),在装置内起初发生的反应为Cu+H2SO4═查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 2NO2(g)(红棕色)???N2O4(g)(无色)△H<0,在平衡后,对平衡体系采取缩小容积、增大压强的措施,因为平衡向正反应方向移动,故体系颜色变浅 | |
| B. | H2(g)+I2(g)???2HI(g)△H<0,在平衡后,对平衡体系采取增大容积、减小压强的措施,因为平衡不移动,故体系颜色不变 | |
| C. | FeCl3+3KSCN???Fe(SCN)3(红色)+3KCl,在平衡后,加少量KCl,因为平衡向逆反应方向移动,故体系颜色变浅 | |
| D. | 对于N2+3H2???2NH3,平衡后,压强不变,充入O2,平衡左移 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | SiO2→H2SiO3 | B. | Cu(OH)2→Fe(OH)3 | C. | CaCO3→Na2CO3 | D. | K2O→KOH |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | NaOH(aq)+HCl(aq)═NaCl(aq)+H2O(l);△H=+28.7 kJ•mol-1 | |
| B. | NaOH(aq)+HCl(aq)═NaCl(aq)+H2O(l);△H=-28.7 kJ•mol-1 | |
| C. | NaOH(aq)+HCl(aq)═NaCl(aq)+H2O(l);△H=+57.4 kJ•mol-1 | |
| D. | NaOH(aq)+HCl(aq)═NaCl(aq)+H2O(l);△H=-57.4 kJ•mol-1 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com