
【题目】NA表示阿伏加德罗常数,则下列说法正确的是
A. 5.6克铁与足量的氯气点燃充分反应,失电子数为2 NA
B. 2.3克金属钠常温下在空气中充分反应和在空气中点燃失电子数之比为1:2
C. 7.8克过氧化钠与足量水反应转移电子数为0.2NA
D. 标况下22.4L纯净的NO2溶于水转移电子数为2NA/3
【答案】D
【解析】
A.铁与氯气反应生成+3价Fe:2Fe+3Cl2![]() 2FeCl3,所以5.6克铁与足量的氯气在点燃条件下充分反应,失电子数为3NA,A项错误;
2FeCl3,所以5.6克铁与足量的氯气在点燃条件下充分反应,失电子数为3NA,A项错误;
B.钠和氧气在常温下或加热时反应,产物不同,但反应中均是金属钠失电子变成钠离子,所以2.3克金属钠常温下在空气中充分反应和在空气中点燃失电子数之比为1:1,B项错误;
C.Na2O2与水反应的化学方程式为:2Na2O2+2H2O=4NaOH+O2,每2molNa2O2反应,转移电子数为2mol,所以0.1molNa2O2反应,转移电子数为0.1NA,C项错误;
D.NO2溶于水发生反应:3NO2+H2O=2HNO3+NO,3molNO2反应,转移的电子数为2mol,所以1mol的NO2完全溶于水,转移的电子数为![]() NA,D项正确;
NA,D项正确;
答案选D项。


科目:高中化学 来源: 题型:
【题目】SiCl4是一种常见的烟雾剂,已知SiCl4的沸点为57.6℃,易挥发和水解。实验室用硅粉与氯气反应制备SiCl4的装置如图所示(夹持装置略去)。
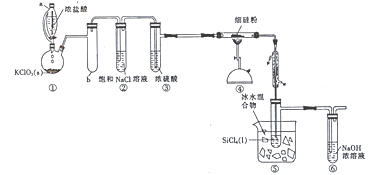
回答下列问题:
(1)装置①中用仪器a代替分液漏斗,其优点是__________________;连接的具支试管b的作用是_____________;氯酸钾与浓盐酸反应的化学方程式为______________________。
(2)实验开始时,先滴入浓盐酸,一段时间后再点燃④中的酒精喷灯,其目的是_____________。
(3)装置⑤的烧杯中用冰水混合物的作用是____________________ 。
(4)某同学认为整套装置中有不足之处,在实验中装置⑤的试管中可能会出现白雾,其原因是______________________ (用化学方程式表示)。请你提出改进的措施:_________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(题文)高铁酸钾(K2FeO4)是一种新型、高效、多功能水处理剂。
(1)工业上的湿法制备方法是用KClO 与Fe(OH)3在KOH 存在下制得K2FeO4,该反应氧化剂与还原剂物质的量之比为_____________。
(2)实验室用食盐、废铁屑、硫酸、KOH等为原料,通过以下过程制备K2FeO4:
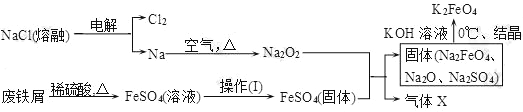
①操作(Ⅰ)的方法为在隔绝空气条件下________、________、过滤、洗涤、隔绝空气减压干燥。
②写出产生X气体的化学方程式_______________________________________。
(3)测定某K2FeO4样品的质量分数,实验步骤如下:
步骤1:准确称量1.0g样品,配制100mL溶液;
步骤2:准确量取25.00mL K2FeO4溶液加入到锥形瓶中;
步骤3:在强碱性溶液中,用过量CrO2-与FeO42-反应生成Fe(OH)3和CrO42-;
步骤4:加稀硫酸,使CrO42-转化为Cr2O72-,CrO2-转化为Cr3+,Fe(OH)3转化为Fe3+;
步骤5:加入二苯胺磺酸钠作指示剂,用0.1000mol·L-1(NH4)2Fe(SO4)2标准溶液滴定至终点(溶液显紫红色),记下消耗(NH4)2Fe(SO4)溶液的体积,做3次平行实验,平均消耗30.00mL的(NH4)2Fe(SO4)2溶液。
已知:K2Cr2O7水溶液显黄色,滴定时发生的反应为:6Fe2++Cr2O72-+14H+==6Fe3++2Cr3++7H2O。
①步骤2中准确量取25.00mLK2FeO4溶液加入到锥形瓶中所用的仪器是________。
②写出步骤3中发生反应的例子方程式___________________________________。
③根据上述实验数据,测定该样品中K2FeO4的质量分数为___________。(K2FeO4摩尔质量为198g/mol)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在一绝热(不与外界发生热交换)的恒容容器中,发生反应:2A(g)+B(s) ![]() C(g)+D(g),下列描述中不能表明反应已达到平衡状态的是( )
C(g)+D(g),下列描述中不能表明反应已达到平衡状态的是( )
A. 混合气体的密度不变 B. 单位时间内生成n molD,同时生成n molC
C. 混合气体的平均相对分子质量不变 D. C(g)的物质的量浓度不变
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列各组离子中,能在溶液中大量共存的是( )
A.Na+、Mg2+、Br-、SO42-B.K+、Ca2+、HCO3-、OH-
C.Fe2+、H+、SO42-、NO3-D.Na+、Cu2+、Cl-、S2-
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列实验不能达到目的的是
A. 用过量NaOH溶液除去镁粉中的铝粉 B. AlCl3溶液和氨水制备Al(OH)3沉淀
C. 用盐酸和AgNO3溶液鉴定Cl- D. 用加热的方法鉴别Na2CO3和NaHCO3
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列叙述正确的是
A.钠燃烧后得到白色的过氧化钠
B.单晶硅可作为光伏电池的材料
C.除去表面氧化膜的铝片在酒精灯上加热会剧烈燃烧
D.新制氯水使pH试纸先变红后褪色,说明其中含HCl和Cl2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某反应中反应物与生成物有:FeCl2、FeCl3、CuCl2、Cu

(1)将上述反应设计成的原电池如图甲所示,请回答下列问题:
①图中X溶液是___________
②Cu电极上发生的电极反应式为__________
③原电池工作时,盐桥中的_____离子(填“K+”或“Cl-”)不断进入X溶液中。
(2)将上述反应设计成的电解池如图乙所示,乙烧杯中金属阳离子的物质的量与电子转移的物质的量的变化关系如图丙,请回答下列问题:
①M是______极;
②图丙中的②线是_________离子的变化。
③当电子转移为2mol时,向乙烧杯中加入_____L5mol/LNaOH溶液才能使所有的金属阳离子沉淀完全。
(3)铁的重要化合物高铁酸钠(Na2FeO4)是一种新型饮用水消毒剂,具有很多优点。
①高铁酸钠生产方法之一是电解法,其原理为Fe+2NaOH+2H2O![]() Na2FeO4+3H2↑,则电解时阳极的电极反应式是__________
Na2FeO4+3H2↑,则电解时阳极的电极反应式是__________
②高铁酸钠生产方法之二是在强碱性介质中用NaClO氧化Fe(OH)3生成高铁酸钠、氯化钠和水,该反应的离子方程式为___________
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com