
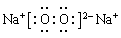 ; 离子键、非极性键(或共价键);
; 离子键、非极性键(或共价键);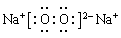 。Na2O2是离子化合物。在Na与O之间以离子键结合,在O、O之间以非极性共价键结合。所以Na2O2中含有的化学键为离子键、非极性键。(4)KO2与CO2发生反应的化学方程式为4KO2 + 2CO2 =2K2CO3 + 3O2;K2O2与CO2反应的方程式为:2K2O2 + 2CO2 =2K2CO3 + O2。若使吸收的CO2与生成的O2体积相同,则n(K2O2):n(KO2)=1:2.
。Na2O2是离子化合物。在Na与O之间以离子键结合,在O、O之间以非极性共价键结合。所以Na2O2中含有的化学键为离子键、非极性键。(4)KO2与CO2发生反应的化学方程式为4KO2 + 2CO2 =2K2CO3 + 3O2;K2O2与CO2反应的方程式为:2K2O2 + 2CO2 =2K2CO3 + O2。若使吸收的CO2与生成的O2体积相同,则n(K2O2):n(KO2)=1:2.

科目:高中化学 来源:不详 题型:单选题
| A.A原子得到电子的数目比B原子少 |
| B.A元素的最高正价比B元素的最高正价要高 |
| C.气态氢化物溶于水后的酸性:A比B强 |
| D.A单质能与B的氢化物水溶液反应,生成B单质 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| W | X | |
| | Y | Z |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.c>b>a | B.a>b>c | C.a>c>b | D.c>a>b |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.ⅠA族与ⅦA族元素间可形成共价化合物或离子化合物 |
| B.第二周期元素从左到右,最高正价从+1递增到+7 |
| C.同主族元素的简单阴离子还原性越强,水解程度越大 |
| D.同周期金属元素的化合价越高,其原子失电子能力越强 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.同周期的主族元素中,ⅦA族元素的原子半径最小 |
| B.碳族元素都是非金属元素,其非金属性随核电荷数的增加而减弱 |
| C.元素周期表中从ⅢB到ⅡB十个纵列的元素都是金属元素 |
| D.ⅠA元素的原子,其半径越大,越容易失去电子 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.钠和镁分别与冷水反应,判断钠和镁的金属活动性强弱 |
| B.在MgCl2与AlCl3溶液中分别加入过量的氨水,判断镁与铝的金属活动性强弱 |
| C.硫酸和硅酸钠溶液反应出白色沉淀,判断硫与硅的非金属活动性强弱 |
| D.Br2与I2分别与足量的H2反应,判断溴与碘的非金属活动性强弱 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.三种元素都是非金属元素 |
| B.Z是地壳中含量最多的元素 |
| C.三种化合物都是共价化合物 |
| D.M、N投入水中所得溶液中溶质相同 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.XYZ | B.X3YZ | C.XYZ2 | D.X2YZ3 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com