
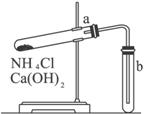
图1
 尖子生新课堂课时作业系列答案
尖子生新课堂课时作业系列答案 英才计划同步课时高效训练系列答案
英才计划同步课时高效训练系列答案科目:高中化学 来源: 题型:阅读理解
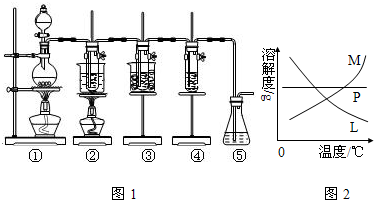
| ||
| ||
查看答案和解析>>
科目:高中化学 来源: 题型:阅读理解

| 高温 |
| 实验步骤 | 操作 | 现象与结论 |
| 第一步 | 取少量液体装于试管,向试 管中滴入几滴KSCN溶液. |
|
| 第二步 | 若溶液紫色褪去,则说明含有Fe2+; 若无明显变化,则说明不含Fe2+. |
查看答案和解析>>
科目:高中化学 来源: 题型:
在实验室,可以用如图7所示的装置制取乙酸乙酯。请回答下列问题:
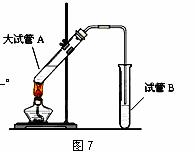
(1)左侧试管中需加浓硫酸做 ▲ 和吸水剂,
右侧试管中盛放的试剂是 ▲ ,
右侧导气管的下端不能插入液面以下,其目的是 ▲ 。
(2)写出实验室用乙醇和乙酸制取乙酸乙酯的化学反应方程式
▲ 。
(3)该反应是典型的可逆反应,若不把生成的乙酸乙酯及时蒸馏 出来,反应一段时间后,
就会达到化学平衡状态。下列能说明该反应已达到化学平衡状态的有(填序号) ▲ 。
①单位时间里,生成1mol乙酸乙酯,同时生成1mol水;
②单位时间里,生成1mol乙酸乙酯,同时生成1mol乙酸;
③单位时间里,消耗1mol乙醇,同时消耗1mol乙酸;
④混合物中各物质的浓度不再变化。
(4)若现有乙酸 90g、乙醇138g发生酯化反应得到66 g乙酸乙酯,试计算该反应的产率为 ▲ 。(产率指的是某种生成物的实际产量与理论产量的比值)
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com