
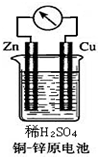
 如图所示的铜-锌原电池中,
如图所示的铜-锌原电池中,分析 铜、锌、稀硫酸构成的原电池中,锌易失电子作负极,铜作正极,负极上失电子发生氧化反应,正极上得电子发生还原反应,根据氧化还原反应方程式设计原电池,失电子的物质作负极;电解质溶液中含有得电子的Ag+,据此分析解答.
解答 解:(1)铜、锌、稀硫酸构成的原电池中,锌易失电子发生氧化反应而作负极,负极上电极反应式为 Zn-2e-=Zn2+,锌片逐渐溶解;铜作正极,正极上氢离子得电子发生还原反应,电极反应式为2H++2e-=H2↑,
故答案为:2H++2e-=H2↑;Zn-2e-=Zn2+;
(2)若生成的氢气在标况下的体积为4.48L,及生成0.2mol氢气,有0.4mol电子转移,原电池加快反应速率;
故答案为:0.4mol;要快;
(3)原电池中失电子的物质作负极,根据反应方程式知,Cu作负极,电解质溶液中含有得电子的Ag+,可用硝酸银溶液作电解质溶液,
故答案为:铜片;硝酸银溶液.
点评 本题考查了原电池原理及原电池的设计,明确正负极上得失电子、反应类型、电极反应式的书写即可解答,难度不大.


科目:高中化学 来源: 题型:选择题
| A. | A、B、C、D的浓度相等 | B. | A、B、C、D在密闭容器中共存 | ||
| C. | A、B、C、D的浓度不再变化 | D. | A消耗的速率与C消耗的速率相等 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

| 容器 | 容积/L | 温度/℃ | 起始量/mol | 平衡量/mol | |
| C(s) | H2O(g) | H2(g) | |||
| 甲 | 2 | T1 | 2 | 4 | 3.2 |
| 乙 | 1 | T2 | 1 | 2 | 1.2 |
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | Li、Be、B原子最外层电子数依次增多 | |
| B. | P、S、Cl元素最高正化合价依次增小 | |
| C. | N、O、F原子半径依次增大 | |
| D. | Na、K、Rb的电子层数依次增多 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 铜片上有气泡产生,发生还原反应 | B. | 锌是负极,发生还原反应 | ||
| C. | 电流方向是从锌片沿导线流向铜片 | D. | 铜片逐渐溶解,被氧化 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
周期 族 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0 |
| 1 | A | |||||||
| 2 | B | C | ||||||
| 3 | D | E | F | G | H | I | ||
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 己烷(己烯) 溴水 分液 | B. | 淀粉溶液(NaCl) 水 过滤 | ||
| C. | CH3CH2OH(CH3COOH) CaO 蒸馏 | D. | CO2(SO2) Na2CO3溶液 洗气 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com