
 �ش��������⣺
�ش��������⣺| ��ѧ�� | C-C | C-H | H-H | C-O | C��O | H-O |
| ���ܣ�kJ/mol�� | 348 | 413 | 436 | 358 | 1072 | 463 |
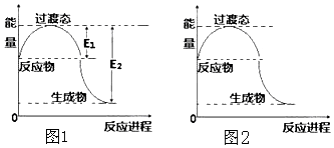
���� ��1��2molCH4��g����4mol O2��g����Ӧ����CO2��g����H2O��g���ų�����368-134=234kJ�������Ȼ�ѧ����ʽ��дԭ�������д��$\frac{18g}{18g/mol}$=1mol����g��l�����ȣ�������1molҺ̬ˮ�ų�����������$\frac{234kJ}{4}$=58.5��
��2����֪����C ��s��ʯī��+O2��g��=CO2��g����H1��
��2H2��g��+O2��g��=2H2O ��l����H2��
��2C2H2��g��+5O2��g���T4CO2��g��+2H2O ��l����H3���١�2+�ڡ�$\frac{1}{2}$-�ۡ�$\frac{1}{2}$�ã�2C ��s��ʯī��+H2��g��=C2H2��g������H=2��H1+$\frac{1}{2}$��H2-$\frac{1}{2}$��H3��
���Ȼ�ѧ����ʽ2C ��s��ʯī��+H2��g��=C2H2��g������H=2��H1+$\frac{1}{2}$��H2-$\frac{1}{2}$��H3���ݴ˽��з�����
��3�����ݻ�ѧ��Ӧ�ʱ�=��Ӧ������ܺ�-����������ܺͼ��㣬��ע���ʾۼ�״̬�Ͷ�Ӧ��Ӧ���ʱ�д���Ȼ�ѧ����ʽ��
��� �⣺��1��2molCH4��g����4mol O2��g����Ӧ����CO2��g����H2O��g���ų�����368-134=234kJ����Ӧ�Ȼ�ѧ����ʽΪ2CH4��g��+4O2��g��=2CO2��g��+4H2O��g����H=-234 kJ•mol-1��$\frac{18g}{18g/mol}$=1mol����g��l�����ȣ�������1molҺ̬ˮ�ų�����������$\frac{234kJ}{4}$=58.5KJ��������������ͷ�Ӧ��Ļ�ܣ���Ӧ���ʼӿ죬ͼ��ӦΪ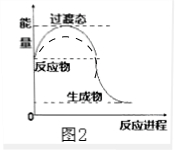 ��
��
�ʴ�Ϊ��2CH4��g��+4O2��g��=2CO2��g��+4H2O��g����H=-234 kJ•mol-1����58.5KJ�� ��
��
��2����֪����C ��s��ʯī��+O2��g��=CO2��g����H1��
��2H2��g��+O2��g��=2H2O ��l����H2��
��2C2H2��g��+5O2��g���T4CO2��g��+2H2O ��l����H3���١�2+�ڡ�$\frac{1}{2}$-�ۡ�$\frac{1}{2}$�ã�2C ��s��ʯī��+H2��g��=C2H2��g������H=2��H1+$\frac{1}{2}$��H2-$\frac{1}{2}$��H3�����Ȼ�ѧ����ʽ2C ��s��ʯī��+H2��g��=C2H2��g������H=2��H1+$\frac{1}{2}$��H2-$\frac{1}{2}$��H3��
�ʴ�Ϊ��2C ��s��ʯī��+H2��g��=C2H2��g������H=2��H1+$\frac{1}{2}$��H2-$\frac{1}{2}$��H3��
��3��CO��g��+2H2��g��?CH3OH ��g������Ӧ���ʱ���Ը��ݷ�Ӧ����ܼ��ܺ���������ܼ��ܼ���õ����ʱ�=��Ӧ���ܼ���֮��-�������ܼ���֮�ͣ�����ͼ���ṩ�Ļ�ѧ���ļ��ܼ���õ�������H1�T1072KJ/mol+2��436KJ/mol-��3��413KJ/mol+358KJ/mol+463KJ/mol��=-116 kJ•mol-1���Ȼ�ѧ����ʽCO��g��+2H2��g��?CH3OH ��g����H=-116 kJ•mol-1��
�ʴ�Ϊ��CO��g��+2H2��g��?CH3OH ��g����H=-116 kJ•mol-1��
���� ���⿼���˻�ѧ��Ӧ�����仯������ͼ���жϺ��Ȼ�ѧ����ʽ��д��������д�Ȼ�ѧ����ʽ�Ļ���Ҫ���ǹؼ�����Ŀ�ϼ�


 ��������ϵ�д�
��������ϵ�д� ���ɶ���ܲ��¿�ֱͨ�߿�ϵ�д�
���ɶ���ܲ��¿�ֱͨ�߿�ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����

| A�� | ��CaC2O4������Һ�м������Na2C2O4������a��䵽b�� | |
| B�� | ͨ������������d��䵽c�� | |
| C�� | d����CaC2O4�������� | |
| D�� | a���Ӧ��Ksp����c���Ӧ��Ksp |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ��ƶ���
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| ʵ��Ŀ�� | ʵ�鷽�� | |
| A | ֤�������鷢����ȥ��Ӧ����ϩ���� | ���Թ��м����������������NaOH���Ҵ���Һ�����ȣ���������������ͨ��������Ȼ�̼��Һ |
| B | ����±������±ԭ�ӵ����� | ��������������������Һ���ȣ�ȡ��ȴ��ӦҺ �μ������ữ��μ���������Һ |
| C | ��֤��Ȳ�ܱ����Ը��������Һ���� | ����ʯ�뱥��ʳ��ˮ��Ӧ���ɵ�����ͨ�����Ը��������Һ���۲���Һ�Ƿ���ɫ |
| D | ��֤����Һ����FeBr3�Ĵ��·���ȡ����Ӧ | ����Ӧ�����Ļ��������ͨ��������Ȼ�̼��Һ��ͨ��AgNO3��Һ�У��۲��Ƿ��е���ɫ�������� |
| A�� | A | B�� | B | C�� | C | D�� | D |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
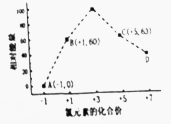 �Ͼ�ӡˢ��·��Ļ������ÿ�ʵ����Դ��������������Ⱦ���Ͼ�ӡˢ��·�徭������룬�ܵõ��ǽ�����ĩ�ͽ�����ĩ��
�Ͼ�ӡˢ��·��Ļ������ÿ�ʵ����Դ��������������Ⱦ���Ͼ�ӡˢ��·�徭������룬�ܵõ��ǽ�����ĩ�ͽ�����ĩ���鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
| Ԫ�� | �����Ϣ |
| X | �ؿ��к�������Ԫ�� |
| Y | Ԫ�ص���̬�⻯�K������ˮ��ˮ��Һ����̪��� |
| Z | �Ǻ�ˮ�г��⡢��Ԫ���⺬������Ԫ�أ��䵥�ʻ���������ˮ���������г��õ������� |
| W | ��Zͬ���ڣ���һ�����������ĵ����ֱܷ��ǣ�I1=578kJ•mol-1��I2=1817kJ•mol-1��I3=2745kJ•mol-1��I4=11575kJ•mol-1 |
| R | �ж��ֻ��ϼۣ�ˮ��Һ�����ɫ���������ڿ����л�Ѹ�ٱ�ɻ���ɫ������ɺ��ɫ |
 ��Z�Ļ�̬ԭ�ӵĵ����Ų�ʽΪ1s22s22p63s23p5��
��Z�Ļ�̬ԭ�ӵĵ����Ų�ʽΪ1s22s22p63s23p5��| �����Ӱ뾶 | ��һ������ | �縺�� | ��̬�⻯���ȶ��� |
| X��Y | X��Y | X��Z | H2X��YH3 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
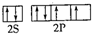
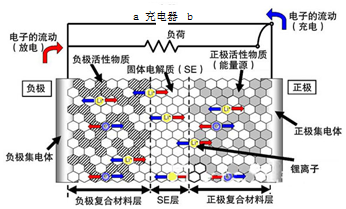 ��һ��ȫ��������ӵ��ʹ������������ʣ����ñ����Ĥ�����ͼ�ѹ���ͼ���������˲��Ͽ���������Ӵ����ԣ��Ӷ�ʵ���������е��ѹ�ij�ŵ磮��صĹ���ԭ��Ϊ��LiMO2+nC$?_{���}^{�ŵ�}$ Li1-xMO2+LixCn ��M������Co��Ni��Fe�ȣ����ڲ��ṹ��ͼ��ʾ�������й�˵����ȷ���ǣ�������
��һ��ȫ��������ӵ��ʹ������������ʣ����ñ����Ĥ�����ͼ�ѹ���ͼ���������˲��Ͽ���������Ӵ����ԣ��Ӷ�ʵ���������е��ѹ�ij�ŵ磮��صĹ���ԭ��Ϊ��LiMO2+nC$?_{���}^{�ŵ�}$ Li1-xMO2+LixCn ��M������Co��Ni��Fe�ȣ����ڲ��ṹ��ͼ��ʾ�������й�˵����ȷ���ǣ�������| A�� | ��طŵ�ʱ�����������ķ�ӦΪ��nC+xLi++xe-�TLixCn | |
| B�� | �������a�˽ӵ�Դ�ĸ�����b�˽ӵ�Դ������ | |
| C�� | ��س��ʱLi+���������ƶ� | |
| D�� | ��ع���ʱ���������������ڶ����� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ��ƶ���
 ��D���ĺ�������Ų�ʽΪ1s2 2s22p6 3s23p6��
��D���ĺ�������Ų�ʽΪ1s2 2s22p6 3s23p6���鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | Na | B�� | Si | C�� | S | D�� | Cl |
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com