
分析 (1)氯气与NaOH反应生成氯化钠、次氯酸钠和水;
(2)发生氧化还原反应生成铁离子,溶液为黄色;
(3)消毒液不能与洁厕灵(主要成分为浓盐酸)混用,发生NaClO+2HCl=NaCl+Cl2↑+H2O,以此计算.
解答 解:(1)氯气与NaOH反应生成氯化钠、次氯酸钠和水,反应为Cl2+2NaOH═NaCl+NaClO+H2O,故答案为:Cl2+NaOH═NaCl+NaClO+H2O;
(2)发生氧化还原反应生成铁离子,溶液为黄色,离子反应方程式为2Fe2++ClO-+2H+═Cl-+2Fe3++H2O,故答案为:2Fe2++ClO-+2H+═Cl-+2Fe3++H2O;
(3)消毒液不能与洁厕灵(主要成分为浓盐酸)混用,发生NaClO+2HCl=NaCl+Cl2↑+H2O,由Cl元素的化合价变化可知,生成1mol氯气转移1mol电子,转移电子个数为6.02×1023或NA,
故答案为:6.02×1023或NA.
点评 本题考查物质的性质,为高频考点,把握物质的性质、发生的反应、氧化还原反应等为解答的关键,侧重分析与应用能力的考查,注意氧化还原反应的应用,题目难度不大.


科目:高中化学 来源: 题型:解答题
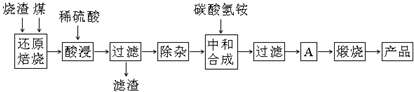
| 氢氧化物 | Al(OH)3 | Mg(OH)2 | Fe(OH)3 | Fe(OH)2 |
| 开始沉淀的pH | 3.10 | 8.54 | 2.01 | 7.11 |
| 完全沉淀的pH | 4.77 | 11.04 | 3.68 | 9.61 |
查看答案和解析>>
科目:高中化学 来源: 题型:推断题
 .C与氢元素可分别形成含10个电子的分子、阴离子和阳离子,阳离子中中心原子的杂化类型为sp3
.C与氢元素可分别形成含10个电子的分子、阴离子和阳离子,阳离子中中心原子的杂化类型为sp3
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 0.5molCl2通入足量水中充分反应.转移的电子数等于0.5NA | |
| B. | 46gNO2和N2O4混合气体中含有原子总数为3NA | |
| C. | 标准状况下,22.4LSO3中含有的分子数为NA. | |
| D. | 1L0.1mol/L的NaHSO3溶液中,HSO32-、SO32-的离子数之和为0.1NA |
查看答案和解析>>
科目:高中化学 来源: 题型:计算题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 25.2g | B. | 18.9g | C. | 23.4g | D. | 48.6g |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 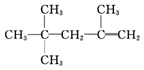 的名称为2,2,4-三甲基-4-戊烯 的名称为2,2,4-三甲基-4-戊烯 | |
| B. | 化合物 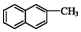 不是苯的同系物 不是苯的同系物 | |
| C. | 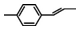 分子中所有碳原子一定共平面 分子中所有碳原子一定共平面 | |
| D. | 除甲酸外的羧酸均不能使高锰酸钾酸性溶液褪色 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
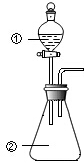 用图所示装置进行下列实验:将①中溶液滴入②中,预测的现象与实际相符的是( )
用图所示装置进行下列实验:将①中溶液滴入②中,预测的现象与实际相符的是( ) | 选项 | ①中物质 | ②中物质 | 预测②中的现象 |
| A | 浓盐酸 | MnO2 | 产生黄绿色气体 |
| B | 浓硝酸 | 用砂纸打磨过的铝条 | 产生红棕色气体 |
| C | 酸化的FeCl2溶液 | H2O2溶液 | 溶液变成黄棕色,有气泡产生 |
| D | Fe2(SO4)3溶液 | 铜粉 | 溶液变蓝色,有黑色固体产生 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com