
| A. | Ba(OH)2溶液与稀硫酸反应:Ba2++OH-+H++SO42-=BaSO4↓+H2O | |
| B. | 用醋酸溶解石灰石:CaCO3+2CH3COOH═Ca2++H2O+CO2↑+2CH3COO- | |
| C. | (NH4)2Fe(SO4)2溶液与过量NaOH溶液反应制Fe(OH)2:Fe2++2OH-=Fe(OH)2↓ | |
| D. | Cu溶于稀硝酸:Cu+2H++NO3=Cu2++NO2↑+H2O |
分析 A.不符合离子的配比;
B.反应生成醋酸钙、水、二氧化碳;
C.与过量NaOH溶液反应,漏写铵根离子与碱的反应;
D.反应生成硝酸铜、NO和水.
解答 解:A.Ba(OH)2溶液与稀硫酸反应的离子反应为Ba2++2OH-+2H++SO42-=BaSO4↓+2H2O,故A错误;
B.用醋酸溶解石灰石的离子反应为CaCO3+2CH3COOH═Ca2++H2O+CO2↑+2CH3COO-,故B正确;
C.(NH4)2Fe(SO4)2溶液与过量NaOH溶液反应制Fe(OH)2的离子反应为2NH4++Fe2++4OH-=Fe(OH)2↓+2NH3•H2O,故C错误;
D.Cu溶于稀硝酸的离子反应为3Cu+8H++2NO3=3Cu2++2NO↑+4H2O,故D错误;
故选B.
点评 本题考查离子反应方程式书写的正误判断,为高频考点,把握发生的反应及离子反应的书写方法为解答的关键,侧重氧化还原反应、复分解反应的离子反应考查,注意离子反应中保留化学式的物质,综合性较强,题目难度不大.


科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

| 离子符号 | Fe3+ | Fe2+ | Cu2+ |
| 氢氧化物开始沉淀时的pH | 2.5 | 7.0 | 4.7 |
| 氢氧化物完全沉淀时的pH | 3.2 | 9.7 | 6.7 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

 这个结构不稳定,自动脱水,生成碳基.
这个结构不稳定,自动脱水,生成碳基. ;有机物C的系统名称为:2-甲基丙醛.
;有机物C的系统名称为:2-甲基丙醛. .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 目前工业废气脱硫应用最广泛的方法是石灰法 | |
| B. | 工业上通过电解熔融的MgCl2获得金属Mg | |
| C. | 钠是一种强还原剂,可以把钛、锆、铌等从其熔融盐中置换出来 | |
| D. | 高炉炼铁的主要反应原理是碳在高温下直接将氧化铁还原成铁 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 原电池中的电极一定要由两种不同的金属组成 | |
| B. | 电子流出的一极是正极 | |
| C. | 任何化学反应都能设计成原电池 | |
| D. | 原电池中的阳离子向正极移动 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 乙醇(水) 加新制的生石灰,过滤 | |
| B. | 乙烷(乙烯) 通过溴的四氯化碳溶液,洗气 | |
| C. | 溴(苯) 加水,振荡,静置后分液 | |
| D. | 乙酸乙酯(乙酸) 加饱和Na2CO3溶液,振荡,静置后分液 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 食醋中含有3-5%的乙酸 | B. | 乙酸可被催化氧化成乙醛 | ||
| C. | 可用乙酸清除水壶中的水垢 | D. | 乙酸分子的官能团是-COOH |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 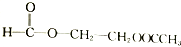 | B. | 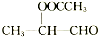 | ||
| C. | 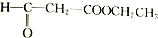 | D. | 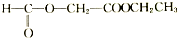 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com