
分析 (1)在25℃、101kPa下,16g甲烷(CH4)的物质的量为1mol,燃烧时消耗2mol氧气生成CO2和液态水时放热890.3kJ,书写热化学方程式时要标明物质的聚集状态;
(2)C (石墨)与足量H2O(g)反应生成CO(g)和H2(g),C(s)+H2O(g)═CO(g)+H2(g),根据n=$\frac{m}{M}$计算24g C 的物质的量为2mol,吸收262.6kJ热量,则1molC,吸收131.3kJ热量,以此书写热化学方程式;
(3)化学反应中,化学键断裂吸收能量,形成新化学键放出能量,根据方程式计算分别吸收和放出的能量,以此计算反应热并判断吸热还是放热.
解答 解:(1)n(CH4)=$\frac{m}{M}$=$\frac{16g}{16g/mol}$=1mol,可知1mol甲烷完全燃烧生成二氧化碳和液态水放热890.3KJ;故燃烧的热化学方程式为:CH4(g)+2O2(g)═CO2(g)+2H2O(l)△H=-890.3kJ•mol-1,
故答案为:CH4(g)+2O2(g)═CO2(g)+2H2O(l)△H=-890.3kJ•mol-1;
(2)24g C 的物质的量为n(C)=$\frac{m}{M}$=$\frac{24g}{12g/mol}$=2mol,2mol碳反应吸收262.6kJ热量,1molC 反应吸收131.3kJ热量,则C (石墨)与足量H2O(g)反应生成CO(g)和H2(g),C(s)+H2O(g)═CO(g)+H2(g)△H=+131.3 kJ•mol-1,
故答案为:C(s)+H2O(g)═CO(g)+H2(g)△H=+131.3 kJ•mol-1;
(3)在反应N2+3H2?2NH3中,断裂3molH-H键,1mol N三N键共吸收的能量为:3×436kJ+946kJ=2254kJ,生成2mol NH3,共形成6mol N-H键,放出的能量为:6×391kJ=2346kJ,吸收的能量少,放出的能量多,该反应为放热反应,放出的热量为:2346kJ-2254kJ=92kJ,即N2(g)+3H2(g)?2NH3(g)△H=-92kJ•mol-1,
故答案为:N2(g)+3H2(g)?2NH3(g)△H=-92kJ•mol-1.
点评 本题主要考查了热化学方程式的书写,需要注意的有:物质的状态、反应热的数值与单位,反应热的数值与化学方程式前面的系数成正比.同时还考查了反应热的计算,题目难度不大,注意把握从键能的角度计算反应热的方法,(3)注意2mol NH3,共形成6mol N-H键,为易错点.


科目:高中化学 来源: 题型:选择题
| 选项 | 目的 | 操作 |
| A | 确定NaCl溶液中是否混有Na2CO3 | 取少量溶液滴加CaCl2溶液,观察是否出现白色浑浊 |
| B | 除去KNO3中少量NaCl | 将混合物制成热的饱和溶液,冷却结晶,过滤 |
| C | 除去硫酸钡固体中的碳酸钡 | 向盛有足量盐酸的烧杯中加入该固体,用玻璃棒不断搅拌并充分浸泡,静置,过滤,洗涤,烘干 |
| D | 配制100mL1.0mol/LCuSO4溶液 | 将25gCuSO4•5H2O溶于100mL蒸馏水中 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| 选项 | A | B |
| 研究目的 | 压强对反应的影响 | 温度对反应的影响 |
| 图示 |  |  |
| 选项 | C | D |
| 研究目的 | 平衡体系中增加N2对反应的影响 | 催化剂对反应的影响 |
| 图示 |  |  |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

| 有关离子 | Fe2+ | Fe3+ | Cr3+ |
| 完全沉淀为对应氢氧化物的pH | 9.0 | 3.2 | 5.6 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 物质(杂质) | 试剂 | 有关离子方程式 |
| NaHCO3(Na2CO3) | ||
| FeCl2(FeCl3) |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
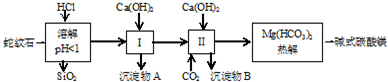
| 氢氧化物 | Fe(OH)3 | Al(OH)3 | Mg(OH)2 |
| 开始沉淀pH | 1.5 | 3.3 | 9.4 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 同温同压下甲和乙的密度之比为1:1 | |
| B. | 等质量的甲和乙中的原子数之比为1:1 | |
| C. | 同温同体积下等质量的甲和乙的压强之比为1:1 | |
| D. | 甲与乙的相对分子质量之比为1:1 |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题

查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com