
下列关于钢铁发生吸氧腐蚀的说法正确的是( )
A.正极上发生的电极反应是2H++2e-—→H2
B.负极上发生的电极反应是Fe2++2e-—→Fe
C.正极上发生的电极反应是2H2O+O2+4e-—→4OH-
D.最终形成黑色的铁锈
科目:高中化学 来源: 题型:
固体氧化物燃料电池是以固体氧化锆—氧化钇为电解质,这种固体电解质在高温下允许氧离子(O2-)在其间通过。该电池的工作原理如下图所示,其中多孔电极a、b均不参与电极反应。
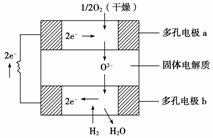
下列判断正确的是( )
A.有O2参加反应的a极为电池的负极
B.b极的电极反应式为H2+O2-—→H2O+2e-
C.a极对应的电极反应式为O2+2H2O+4e-—→4OH-
D.该电池的总反应式为2H2+O2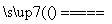 2H2O
2H2O
查看答案和解析>>
科目:高中化学 来源: 题型:
已知: ,从A出发发生图示中的一系列反应,其中B和C按1:2反应生成Z,F和E按1:2反应生成W,W和Z互为同分异构体。
,从A出发发生图示中的一系列反应,其中B和C按1:2反应生成Z,F和E按1:2反应生成W,W和Z互为同分异构体。
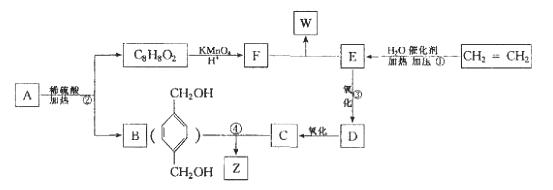
回答下列问题:
(1)写出反应类型:①_____________________,②______________________________。
(2)写出下列反应的化学方程式:
③_____________________________________________________;
④_____________________________________________________。
(3)与B互为同分异构体,属于酚类且苯环上只有两个互为对位取代基的化合物有4种,其结构简式为_______________,_________________,_______________,______________。
(4)A的结构简式可能为_______________________________________(只写一种即可)。
查看答案和解析>>
科目:高中化学 来源: 题型:
下列有关金属腐蚀与防护的说法正确的是( )
①纯银器表面在空气中因化学腐蚀渐渐变暗 ②当镀锡铁制品的镀层破损时,镀层仍能对铁制品起保护作用 ③在海轮外壳连接锌块保护外壳不受腐蚀是采用了牺牲阳极的阴极保护法 ④可将地下输油钢管与外加直流电源的正极相连以保护它不受腐蚀
A.①③ B.②③ C.①④ D.②④
查看答案和解析>>
科目:高中化学 来源: 题型:
如何防止铁的锈蚀是工业上研究的重点内容。为研究铁锈蚀的影响因素,某同学做了如下探究实验:
| 序号 | 内容 | 实验现象 |
| 1 | 常温下将铁丝放在干燥空气中一个月 | 干燥的铁丝表面依然光亮 |
| 2 | 常温下将铁丝放在潮湿空气中一小时 | 铁丝表面依然光亮 |
| 3 | 常温下将铁丝放在潮湿的空气中一个月 | 铁丝表面已变得灰暗 |
| 4 | 将潮湿的铁丝放在常温的氧气流中一小时 | 铁丝表面略显灰暗 |
| 5 | 将潮湿的铁丝放在高于常温的氧气流中一小时 | 铁丝表面已变得灰暗 |
| 6 | 将浸过氯化钠溶液的铁丝放在高于常温的氧气流中一小时 | 铁丝表面灰暗程度比实验5严重 |
回答以下问题:
(1)上述实验中发生了电化学腐蚀的是(填实验序号)____________;在电化学腐蚀中,负极反应是_________________________________________________________________;
正极反应是__________________________________________________________;
(2)由该实验可知,可以影响铁锈蚀速率的因素是
________________________________________________________________________;
(3)为防止铁的锈蚀,工业上普遍采用的方法是____________________(答两种方法)。
查看答案和解析>>
科目:高中化学 来源: 题型:
将0.20 mol NO和0.1 mol CO充入一个容积恒定为1L的密闭容器中发生反应:
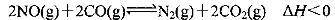
在不同条件下,反应过程中部分物质的浓度变化如图所示。
下列说法正确的是
A.容器内的压强不发生变化说明该反应达到平衡
B.当向容器中再充入0.20 mol NO时,平衡向正反应方
向移动,K增大
C.第12 min时改变的反应条件为升高温度
D.向该容器内充入He气,容器内气体压强增大,所以
反应速率增大
查看答案和解析>>
科目:高中化学 来源: 题型:
常温下,下列各溶液的叙述中正确的是
A. NaHSO3与Na2SO3混合溶液中:3c(Na+)=c(HSO3-)+c(SO32-)
B. 0.1 mol/L 的醋酸钠溶液20 mL与0.1 mol/L盐酸10mL 混合后溶液显酸性:
c(CH3COO-)>c(CH3COOH)>c(Cl-)>c(H+)
C. 等物质的量浓度等体积的NH4HSO4和NaOH溶液混合:
c(Na+)=c(SO42-) >c ( NH4+)> c(H+)>c(OH-)
D. 向1.00L 0.3 mol/L NaOH溶液中缓慢通入0.2 mol CO2气体,溶液中:
c(Na+)>c(CO32-) >c(HCO3-)>c(OH-)> c(H+)
查看答案和解析>>
科目:高中化学 来源: 题型:
实验室用乙酸和正丁醇制备乙酸正丁酯。有关物质的相关数据如下表:
| 化合物 | 相对分子质量 | 密度/g·cm-3 | 沸点,/℃ | 溶解度/l00g水 |
| 正丁醇 | 74 | 0.80 | 118.0 | 9 |
| 冰醋酸 | 60 | 1.045 | 118.1 | 互溶 |
| 乙酸正丁酯 | 116 | 0.882 | 126.1 | 0.7 |
操作如下:
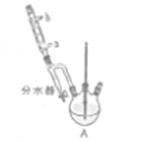
①在50mL三颈烧瓶中,加入18.5 mL正丁醇和13.4 mL冰醋酸, 3~4滴浓硫酸,投入沸石。安装分水器(作用:实验过程中不断分离除去反应生成的水)、温度计及回流冷凝管。
②将分水器分出的酯层和反应液一起倒入分液漏斗中,水洗,10% Na2CO3洗涤,再水洗,最后转移至锥形瓶,干燥。
③将干燥后的乙酸正丁酯滤入烧瓶中,常压蒸馏,收集馏分,得15.1 g乙酸正丁酯。
请回答有关问题:
(1)冷水应该从冷凝管 (填a或b)端管口通入。
(2)仪器A中发生反应的化学方程式为____ 。
(3)步骤①“不断分离除去反应生成的水”该操作的目的是: 。
(4)步骤②中,10%Na2CO3溶液洗涤有机层,该步操作的目的是 。
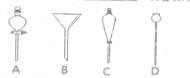
(5)进行分液操作时,使用的漏斗是 (填选项)。
(6)步骤③在进行蒸馏操作时,若从118℃开始收集馏分,产率偏 (填“高”或者“低”)原因是____
(7)该实验过程中,生成乙酸正丁酯的产率是 。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com