


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
| 催化剂 |
| △ |

查看答案和解析>>
科目:高中化学 来源: 题型:
 在常温常压下,可利用下列装置来测定气体体积,抽气装置E用以调节装置中的气压差,减小实验误差.
在常温常压下,可利用下列装置来测定气体体积,抽气装置E用以调节装置中的气压差,减小实验误差.查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
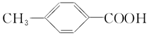 )是一种广泛应用于制备止血芳酸、农药杀虫剂、感光材料的白色晶体,已知其有多种同分异构体,其中属于酯类(分子结构形式为:
)是一种广泛应用于制备止血芳酸、农药杀虫剂、感光材料的白色晶体,已知其有多种同分异构体,其中属于酯类(分子结构形式为: ,R为烃基或H,R′为烃基),且分子结构中含有甲基和苯环的同分异构体的种数为( )
,R为烃基或H,R′为烃基),且分子结构中含有甲基和苯环的同分异构体的种数为( )| A、3种 | B、4种 | C、5种 | D、6种 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、周期表中的主族都有非金属元素 |
| B、周期表中的主族都有金属元素 |
| C、周期表中的非金属元素都位于短周期 |
| D、周期表中的过渡元素都是金属元素 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、pH为1的无色溶液:Fe2+、SO32-、Cl- |
| B、使碘化钾淀粉试纸变蓝的溶液:Na+、NH4+、S2-、Br- |
| C、碱性溶液中:Ba2+、Na+、NO3-、Cl- |
| D、加入铝条有氢气放出的溶液:Na+、NH4+、HCO3-、SO42- |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、25% | B、50% |
| C、63.2% | D、75% |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com