
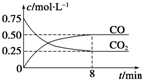
 某温度下,在一密闭容器中充入一定量CO2,并加入足量铁粉,发生反应:Fe(s)+CO2(g)?FeO(s)+CO(g),测得CO2和CO浓度随时间的变化如图所示:
某温度下,在一密闭容器中充入一定量CO2,并加入足量铁粉,发生反应:Fe(s)+CO2(g)?FeO(s)+CO(g),测得CO2和CO浓度随时间的变化如图所示:| 温度/K | K1 | K2 |
| 973 | 1.47 | 2.38 |
| 1173 | 2.15 | 1.67 |
分析 (1)0~8min,v(CO)=$\frac{△c}{△t}$;
(2)能够改变平衡时c(CO)/c(CO2)的比值说明平衡发生移动或加入两种物质中的一种;
(3)i.Fe(s)+CO2(g)?FeO(s)+CO(g),K1=$\frac{c(CO)}{c(C{O}_{2})}$
ii.Fe(s)+H2O(g)?FeO(s)+H2(g),K2=$\frac{c({H}_{2})}{c({H}_{2}O)}$
方程式i-ii得CO2(g)+H2(g)?CO(g)+H2O(g)则K=$\frac{c(CO).c({H}_{2}O)}{c(C{O}_{2}).c({H}_{2})}$=$\frac{{K}_{1}}{{K}_{2}}$,
据此计算不同温度下的K值,
升高温度,化学平衡向吸热方向移动.
解答 解:(1)0~8min,v(CO)=$\frac{△c}{△t}$=$\frac{0.50mol/L-0}{8min}$=0.0625mol/(L.min),故答案为:0.0625;
(2)能够改变平衡时c(CO)/c(CO2)的比值说明平衡发生移动或加入两种物质中的一种,
A.升高温度反应向吸热方向移动,则该比值一定发生变化,故A正确;
B.Fe粉的量改变,不改变浓度,平衡不移动,则该比值不发生变化,故B错误;
C.改变压强,平衡不移动,则该比值不发生变化,故C错误;
D.改变CO的量平衡发生移动,所以该比值发生变化,故D正确;
故选AD;
(3)i.Fe(s)+CO2(g)?FeO(s)+CO(g),K1=$\frac{c(CO)}{c(C{O}_{2})}$
ii.Fe(s)+H2O(g)?FeO(s)+H2(g),K2=$\frac{c({H}_{2})}{c({H}_{2}O)}$
方程式i-ii得CO2(g)+H2(g)?CO(g)+H2O(g)则K=$\frac{c(CO).c({H}_{2}O)}{c(C{O}_{2}).c({H}_{2})}$=$\frac{{K}_{1}}{{K}_{2}}$,
①温度为973K时:K=$\frac{1.47}{2.38}$=0.62,故答案为:0.62;
②温度为1173K时:K=$\frac{2.15}{1.67}$=1.29,故答案为:1.29;
③升高温度,该反应的化学平衡常数增大,则该反应向正反应方向移动,升高化学平衡向吸热方向移动,所以正反应是吸热反应,故答案为:吸热.
点评 本题考查化学平衡有关计算,侧重考查学生分析计算能力,明确各个物理量之间的关系式是解本题关键,注意(3)中总方程式K不等于K1+K2.


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:选择题
| A. | 用醋酸除去水垢:CaCO3+2H+═Ca2++H2O+CO2↑ | |
| B. | 用小苏打治疗胃酸过多:HCO3-+H+═CO2↑+H2O | |
| C. | 锌片插入硝酸银溶液中:Zn+Ag+═Zn2++Ag | |
| D. | 硫酸溶液与氢氧化铜反应:H++OH-═H2O |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
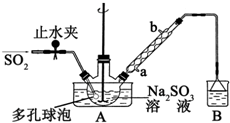 次硫酸氢钠甲醛(NaHSO2•HCHO•2H2O)俗称吊白块,不稳定,120℃时会分解,在印染、医药以及原子能工业中有广泛应用.以Na2SO3、SO2、HCHO和锌粉为原料制备次硫酸氢钠甲醛的实验步骤如图:
次硫酸氢钠甲醛(NaHSO2•HCHO•2H2O)俗称吊白块,不稳定,120℃时会分解,在印染、医药以及原子能工业中有广泛应用.以Na2SO3、SO2、HCHO和锌粉为原料制备次硫酸氢钠甲醛的实验步骤如图:查看答案和解析>>
科目:高中化学 来源: 题型:解答题
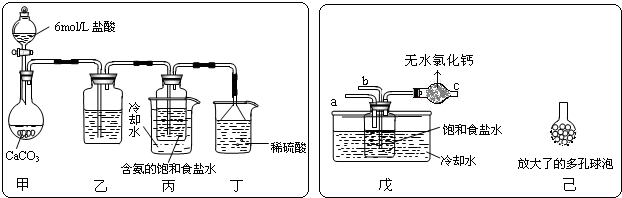
查看答案和解析>>
科目:高中化学 来源: 题型:实验题

| 开始沉淀时的pH | 沉淀完全时的pH | |
| Mg2+ | 9.6 | 11.0 |
| Ca2+ | 12.2 | c(OH-)=1.8mol•L-1 |
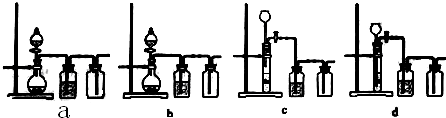
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
 | 相对分子质量 | 密度/g•cm-3 | 沸点/℃ | 水中溶解性 | |
| 乙酸 | 60 | 1.051 | 118.0 | 溶 | |
| 环己醇 | 100 | 0.982 | 160.8 | 微溶 | |
| 乙酸环己酯 | 142 | 0.969 | 173.5 | 难溶 |
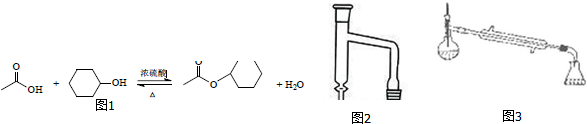
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
 实验室制备1,2二溴乙烷的反应原理如下:
实验室制备1,2二溴乙烷的反应原理如下:| 乙醇 | 1,2二溴乙烷 | 乙醚 | |
| 状态 | 无色液体 | 无色液体 | 无色液体 |
| 密度/g•cm-3 | 0.79 | 2.2 | 0.71 |
| 沸点/℃ | 78.5 | 132 | 34.6 |
| 熔点/℃ | -130 | 9 | -116 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com