
| A. | NaHCO3属于酸式盐,其水溶液显酸性 | |
| B. | CuCl2水解的实质是Cu2+与水电离出来的OH-结合生成了弱电解质Cu(OH)2 | |
| C. | 利用纯碱水解显碱性,可除去物品表面的油污 | |
| D. | 明矾【KAl(SO4)2•12H2O】用于净水的原因是明矾电离产生的Al3+水解产生Al(OH)3胶体,Al(OH)3胶体吸附水中悬浮的杂质. |
分析 A.碳酸氢钠溶液中碳酸氢根离子水解大于电离溶液显碱性;
B.盐类水解实质是弱离子结合水电离出的氢氧根离子或氢离子生成弱电解质,促进水的电离平衡正向进行;
C.纯碱是碳酸钠,溶液中碳酸根离子水解溶液显碱性,油脂在碱溶液中水解生成溶于水的物质;
D.明矾【KAl(SO4)2•12H2O】用于净水的原因是溶液中铝离子水解生成氢氧化铝胶体具有吸附悬浮杂质的作用;
解答 解:A.NaHCO3属于酸式盐,溶液中碳酸氢根离子水解程度大于其电离程度,其水溶液显碱性,故A错误;
B.CuCl2水解的实质是Cu2+与水电离出来的OH-结合生成了弱电解质Cu(OH)2,促进水的电离平衡正向进行,溶液显酸性,故B正确;
C.碳酸钠溶液中碳酸根离子水解溶液显碱性,油脂在碱溶液中水解生成溶于水的物质,利用纯碱水解显碱性,可除去物品表面的油污,故C正确;
D.明矾净水的原因是明矾电离产生的Al3+水解产生Al(OH)3胶体,Al(OH)3胶体吸附水中悬浮的杂质,故D正确;
故选A.
点评 本题考查了盐类水解的原理和实质、溶液酸碱性的分析判断,掌握基础是解题关键,题目难度中等.


 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源: 题型:选择题
| A. | K+、OH-、CO32- | B. | Na+、Cl-、Ag+ | C. | K+、SO42-、S2- | D. | H+、Cu2+、NO3- |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
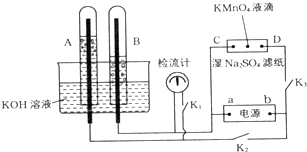
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 晶体中有阳离子存在,就一定存在阴离子 | |
| B. | 离子键没有饱和性和方向性,但阴阳离子的配位数并不是任意的 | |
| C. | 电负性相差不大的两个原子,只要有未成对电子,就一定能形成共价键 | |
| D. | 如果分子间形成了氢键,物质的密度就会增大 |
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | NaHCO3溶液和过量NaOH溶液混合HCO3-+OH-=CO32-+H2O | |
| B. | 在氢氧化钠溶液中滴加少量氯化铝 Al3++3OH-=Al(OH)3↓ | |
| C. | 将少量稀盐酸滴加到碳酸钠溶液中:2H++CO32-=H2O+CO2↑ | |
| D. | 向硫酸铝钾溶液中滴加氢氧化钡溶液至沉淀物质的量最多3Ba2++6OH-+2Al3++3SO42-═3BaSO4↓+2Al(OH)3↓ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ①③ | B. | ②④ | C. | ①② | D. | ③④ |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com