
【题目】关于氯化铁溶液,下列有关说法正确的是( )
A.适当升高温度能促进FeCl3水解
B.加水稀释能促进其水解,并提高Fe(OH)3的浓度
C.加少量浓盐酸能促进FeCl3水解
D.保存氯化铁溶液时应加入少量铁粉
 名师导航单元期末冲刺100分系列答案
名师导航单元期末冲刺100分系列答案 名校名卷单元同步训练测试题系列答案
名校名卷单元同步训练测试题系列答案科目:高中化学 来源: 题型:
【题目】甲醛(CH2O)、乙酸(C2H4O2)和丙醛(C3H6O)组成的混合物中,氧元素的质量分数是37%,则碳元素的质量分数为
A. 27% B. 28% C. 54% D. 无法计算
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】将等物质的量浓度的CuSO4溶液和NaCl溶液等体积混合后,用石墨电极进行电解,电解过程中,溶液pH随时间t变化的曲线如下图,则下列说法正确的是( )

A. 阳极产物一定是Cl2,阴极产物一定是Cu
B. BC段表示在阴极上是H+放电产生了H2
C. 整个过程中阳极先产生Cl2,后产生O2
D. CD段表示阳极上OH一放电破坏了水的电离平衡,产生了H+
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】0.1moL/L醋酸用蒸馏水稀释的过程中,下列说法正确的是( )
A.电离程度增大,H+浓度增大B.电离程度减小,H+浓度减小
C.电离程度增大,H+浓度减小D.电离程度减小,H+浓度增大
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】实验室用氯化钠固体配制1.00mol/L的NaCl溶液0.5L,回答下列问题.
(1)请写出该实验的实验步骤
①溶解 ②冷却 ③转移 ④⑤⑥摇匀
(2)现在已有下列仪器:托盘天平,烧杯,量筒,要完成本实验还需仪器为:、 .
(3)试分析下列操作对所配溶液的浓度有何影响(偏高、偏低或者无影响)及造成该影响的原因.
①容量瓶用蒸馏洗涤后残留有少量的水,对所配溶液浓度的影响 , 原因是:
②定容后,加盖倒转摇匀后,发现液面低于刻度线,又滴加蒸馏水至刻度.对所配溶液浓度的影响 , 原因是: .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氨气及含氮化合物在化工生产和国防工业中具有广泛应用。请回答:
(1)已知:(i)氢气的燃烧热为286.0 kJ mol-1
(ii)4NH3(g)+3O2(g)![]() 2N2(g)+6H2O △H=-1530.6kJmol-1。
2N2(g)+6H2O △H=-1530.6kJmol-1。
①合成氨反应的热化学方程式为__________________________________。
②对于反应(ii),正、逆反应活化能的大小关系为:E正_______E逆 (填>、=或<)。
(2)恒温恒容条件下,起始按物质的量之比为1 : 1向密闭容器中充入N2(g)和H2(g),发生合成氨的反应。达平衡后,N2(g)的体积分数为_________;然后只降低温度,N2(g)的体积分数会______(填选项字母)。
A.增大 B.减小 C.不变 D.不能判断
(3)T℃ 时,CO2(g)和 NH3(g)合成尿素的原理为 2NH3(g)+ CO2(g)![]() CO(NH2)2(s)+H2O(l)。在2 L恒容密闭容器中,通入1.2 mol NH3(g)和0.6 mol CO2(g),2 min时反应恰好达到平衡,测得c(NH3)=0.2mol L-1
CO(NH2)2(s)+H2O(l)。在2 L恒容密闭容器中,通入1.2 mol NH3(g)和0.6 mol CO2(g),2 min时反应恰好达到平衡,测得c(NH3)=0.2mol L-1
①0-2 min内,用NH3表示的反应速率v(NH3)=___________;反应的平衡常数K=__________。
②若其他条件不变,2 min时将容器体积迅速压缩到1 L,在3 min时重新达到平衡,请在图1中画出23 min内c(NH3)随时间(t)变化的曲线关系图:__________。

(4)电化学降解法可用于治理水中硝酸盐的污染,电化学降解NO3-的原理如图2所示:
①电源正极为___________(填“A”或“B”),阴极反应式为________________________________。
②若电解过程中转移了 1 mol e-,则膜两侧电解液的质量变化差值(Δm正-Δm右)为________g。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在溶液中,反应![]()
![]() C分别在三种不同实验条件下进行,它们的起始状态均为:
C分别在三种不同实验条件下进行,它们的起始状态均为: ![]() 、
、![]() 、
、![]() 。在三种条件下,反应物A的浓度随时间的变化如图所示。下列说法中正确的是( )
。在三种条件下,反应物A的浓度随时间的变化如图所示。下列说法中正确的是( )
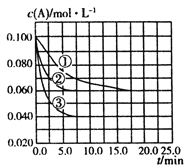
A. 反应的平衡常数:①<②
B. 反应A+2B![]() C的
C的![]()
C. 实验②平衡时B的转化率为60%
D. 实验③平衡时![]()
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com