
| A. | 1mol•L-1K2SO4溶液中含有钾离子数为2NA | |
| B. | 0.1mol铁与0.1mol氯气点燃完全反应,转移电子数为0.3NA | |
| C. | 常温常压下,6.4g氧气和臭氧混合气体中含有的原子总数为0.4NA | |
| D. | 1L1mol•L-1氨水中,含有的NH3与NH3•H20分子的总数为NA |
分析 A.缺少硫酸钾溶液的体积,无法计算钾离子的数目;
B.氯气不足,0.1mol氯气完全反应转移0.2mol电子;
C.氧气和臭氧分子中都只含有氧元素,6.4g混合物中含有6.4g氧原子,含有0.4mol氧原子;
D.根据混合液中的物料守恒判断.
解答 解:A.没有告诉1mol•L-1K2SO4溶液的体积,无法计算溶液中钾离子的物质的量,故A错误;
B.0.1mol铁与0.1mol氯气点燃完全反应,氯气不足,0.1mol氯气完全反应转移0.2mol电子,转移电子数为0.2NA,故B错误;
C.6.4g氧气和臭氧的混合物中含有6.4g氧原子,含有氧原子的物质的量为:$\frac{6.4g}{16g/mol}$=0.4mol,含有的原子总数为0.3NA,故C错误;
D.1L 1mol•L-1氨水中,含有溶质一水合氨1mol,根据物料守恒含有的NH3与NH3•H20分子的总物质的量为1mol,NH3与NH3•H20分子的总数为NA,故D正确;
故选D.
点评 本题考查阿伏加德罗常数的综合应用,题目难度中等,注意掌握好以物质的量为中心的各化学量与阿伏加德罗常数的关系,准确弄清分子、原子、原子核内质子中子及核外电子的构成关系,A为易错点,注意题中缺少溶液体积.


 名题金卷系列答案
名题金卷系列答案科目:高中化学 来源: 题型:选择题
| A. | Fe304与稀硝酸反应的离子方程式为:3Fe3O4+28H++N03一═9Fe3++NO↑+14H20 | |
| B. | 用稀硫酸除去铜绿:4H++Cu2(OH)2CO3═2Cu2++C02↑+3H2O | |
| C. | 向NH4Al(S04)2溶液中滴人Ba(OH)2溶液恰好使S042-完全沉淀:2Ba2-+NH4++Al3++2SO42-+40H-═Al(OH)3↓+NH3•H20+2BaSO4↓ | |
| D. | 少量氢氧化钙溶液与碳酸氢钠溶液混合:Ca2++OH-+HC03-═CaCO3↓+H2O |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 厕所清洁剂、厨房清洁剂、醋、肥皂 | B. | 醋、厕所清洁剂、肥皂、厨房清洁剂 | ||
| C. | 厕所清洁剂、醋、肥皂、厨房清洁剂 | D. | 厨房清洁剂、醋、肥皂、厕所清洁剂 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | pH=0的溶液中:Fe3+、Mg2+、Cl-、SO42- | |
| B. | 在含大量Al3+的溶液中:Na+、K+、AlO2-、NO3- | |
| C. | 滴入甲基橙指示剂呈红色的溶液中:Na+、NH4+、CO32-、NO3- | |
| D. | 水电离出的c(H+)=1×10-13mol•L-1的溶液中:K+、HCO3-、Cl-、NH4+ |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
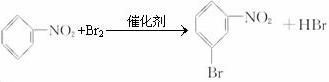 、
、 、
、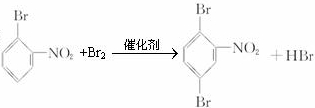 或
或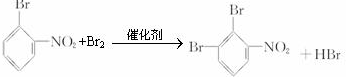 .
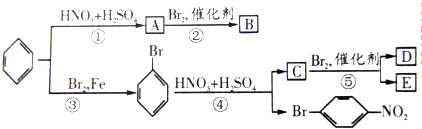
.
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ② | B. | ①③⑤ | C. | ②④ | D. | ②③⑤ |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
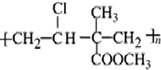 ,其单体为:CH2=CHCl、CH2=C(CH3)COOCH3.
,其单体为:CH2=CHCl、CH2=C(CH3)COOCH3.查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com