
 �� ��������
�� �������� ��
��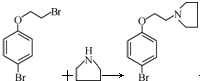 +HBr
+HBr ��
��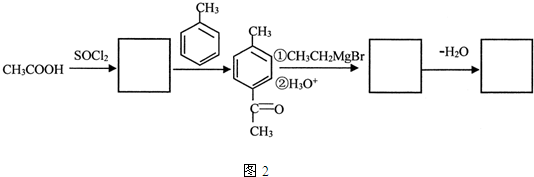
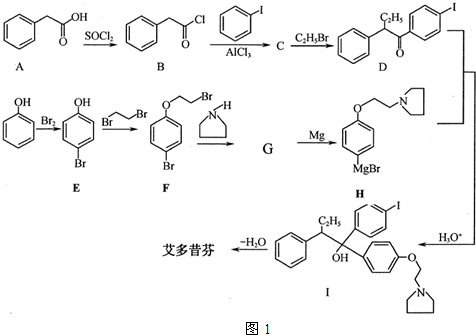
���� �������и�����ת����ϵ�����ո������й����ŵı仯��̼���ṹ�ı仯������
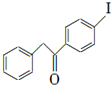
��1���Ƚ�B��D�������ʵĽṹ������֮��������Ӧ��������֪C�Ľṹ��ʽ��I�е��ǻ�����λ̼�ϵ���ԭ����ȥһ����ˮ�ð������ң�
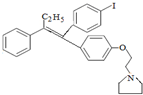
��2���Ƚ�F��H�������ʵĽṹ��ʽ��֪G�Ľṹ��ʽΪ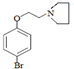 ����������д����ѧ����ʽ��
����������д����ѧ����ʽ��
��3�����ݢ��ܷ���������Ӧ��˵����ȩ�����ڷ��ӵĺ˴Ź�������ͼ����4���壻���ܷ���ˮ�ⷴӦ�Ҳ���֮һ��FeCl3��Һ�ܷ�����ɫ��Ӧ��˵��ˮ�����֮һ�з��ǻ����ݴ�дͬ���칹�壻
��4���Լױ���SOCl2��Ӧ������A��B�ķ�Ӧ������ȡ����Ӧ����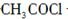 ��
��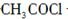 ��ױ�����ȡ����Ӧ��
��ױ�����ȡ����Ӧ��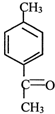 ��
�� ����CH3CH2MgBr��������D+H��I�ķ�Ӧ��Ȼ������ˮ�γ�̼̼˫����
����CH3CH2MgBr��������D+H��I�ķ�Ӧ��Ȼ������ˮ�γ�̼̼˫����
��� �⣺��1���Ƚ�B��D�������ʵĽṹ������֮��������Ӧ��������֪��B��C�ķ�ӦΪB�е���ԭ����ⱽ�е�Ķ�λ��ԭ�ӽ�ϣ������ⱽ����ȡ��������C�Ľṹ��ʽΪ ��I�е��ǻ�����λ̼�ϵ���ԭ����ȥһ����ˮ�ð������ң����������ҵĽṹ��ʽΪ
��I�е��ǻ�����λ̼�ϵ���ԭ����ȥһ����ˮ�ð������ң����������ҵĽṹ��ʽΪ ��
��
�ʴ�Ϊ�� ��
�� ��
��
����I�Ľṹ��ʽ��֪��I�к����ǻ����Ѽ���
�ʴ�Ϊ���ǻ����Ѽ���
��2���Ƚ�F��H�������ʵĽṹ��ʽ��֪G�Ľṹ��ʽΪ ������F��G�Ļ�ѧ����ʽΪ
������F��G�Ļ�ѧ����ʽΪ +HBr��
+HBr��
�ʴ�Ϊ�� +HBr��
+HBr��
��3�����ݢ��ܷ���������Ӧ��˵����ȩ�����ڷ��ӵĺ˴Ź�������ͼ����4���壻���ܷ���ˮ�ⷴӦ�Ҳ���֮һ��FeCl3��Һ�ܷ�����ɫ��Ӧ��˵��ˮ�����֮һ�з��ǻ���������Щ������ͬ���칹���� ��
��
�ʴ�Ϊ�� ��
��
��4���Լױ���SOCl2��Ӧ������A��B�ķ�Ӧ������ȡ����Ӧ����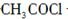 ��
��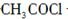 ��ױ�����ȡ����Ӧ��
��ױ�����ȡ����Ӧ�� ��
�� ����CH3CH2MgBr��������D+H��I�ķ�Ӧ���õ�����Ϊ
����CH3CH2MgBr��������D+H��I�ķ�Ӧ���õ�����Ϊ ��
�� ��ˮ�γ�̼̼˫���õ�����Ϊ
��ˮ�γ�̼̼˫���õ�����Ϊ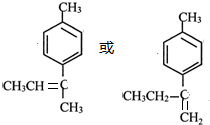 ��
��
�ʴ�Ϊ��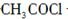 ��
�� ��
�� ��
��
���� ������Ҫ�������л���֮����ת�����л�������ʣ��Ѷ��еȣ�����ʱע���л����������ʵ����Ӧ���Լ�������Ϣ���Ͻ��������ƶϣ�������ѵ��ǵڣ�5���ʣ��ۺ��Խ�ǿ����ѧ���ۺϷ�������������ϸߣ�



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ��C��s��ʯī����C��s�����ʯ��-1.9 kJ����֪��ʯī�Ƚ��ʯ���ȶ� | |
| B�� | ���������������������ֱ���ȫȼ�գ����߷ų����������� | |
| C�� | ��H+��aq��+OH-��aq����H2O��l��+57.3 kJ����֪����1 mol CH3COOH����Һ�뺬1 mol NaOH����Һ��ϣ��ų���������57.3 kJ | |
| D�� | 2 g H2��ȫȼ������Һ̬ˮ�ų�285.8 kJ������������ȼ�յ��Ȼ�ѧ����ʽΪ2H2��g��+O2��g����2H2O��l��+285.8 kJ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ����Ӧ�Ļ�ܱ��淴Ӧ�Ļ�ܴ�234kJ•mol-1 | |
| B�� | NO3�Ǹ÷�Ӧ�Ĵ��� | |
| C�� | ��ѧ��Ӧ����v��NO2��=2v��CO�� | |
| D�� | ����1����2��Ϊ���ȷ�Ӧ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ��ϩ���Ҵ��� | B�� | ˳����ʯ���ѽ����� | ||
| C�� | �⣨������ | D�� | �壨��ˮɹ�κ����Һ�� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ���ѡ��
| A�� | Na3PO4 | B�� | Na4P2O7 | ||
| C�� | Na4P2O7 ��Na5P3O10 | D�� | Na3PO4��Na4P2O7��Na5P3O10 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | �����ͺ�ֲ���Ͷ�����ͨ��ʯ�ͷ�������ȡ | |
| B�� | ��������������Ѫ����ɳɷ� | |
| C�� | �����ʵ�ˮ����ﶼ�Ǧ�-������ | |
| D�� | ���PM2.5��ֱ��ԭ��������ɳĮ�� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
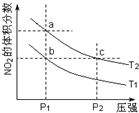 ��Ӧ2NO2��g��?N2O4��g��+57kJ���������������������䣮���¶�ΪT1��T2ʱ��ƽ����ϵ��NO2�����������ѹǿ�仯������ͼ��ʾ������˵����ȷ���ǣ�������
��Ӧ2NO2��g��?N2O4��g��+57kJ���������������������䣮���¶�ΪT1��T2ʱ��ƽ����ϵ��NO2�����������ѹǿ�仯������ͼ��ʾ������˵����ȷ���ǣ�������| A�� | a��c�����������ɫ��adz��c�� | |
| B�� | a��c���������ƽ����Է���������a��c | |
| C�� | b��c�����ƽ�ⳣ����Kb=Kc | |
| D�� | ״̬aͨ�������¶ȿɱ��״̬b |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
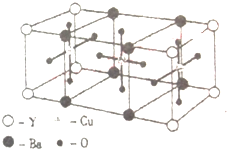 ��֪ij������ľ�������������С��Ԫ���öѻ����ɵģ����ڸû������������������ȷ���ǣ�������
��֪ij������ľ�������������С��Ԫ���öѻ����ɵģ����ڸû������������������ȷ���ǣ�������| A�� | �û�����Ļ�ѧʽ��Y4Ba4Cu3O12 | B�� | �û�����Ļ�ѧʽ��YBaCu3O6 | ||
| C�� | �û�����Ļ�ѧʽ��Y2BaCu3O6 | D�� | �û�����Ļ�ѧʽ��YBa2Cu3O7 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com