
| A. | 原子核外每一个能层最多可容纳的电子数为n2 | |
| B. | 任一能层的能级总是从s能级开始,而且能级数等于该能层序数 | |
| C. | 同是s能级,在不同的能层中所能容纳的最多电子数是不相同的 | |
| D. | 1个原子轨道里最多只能容纳2个电子,且自旋方向相同 |
分析 A、根据核外电子排布规律:各电子层最多容纳电子数2n2(n为电子层数);
B、根据能层与能级的关系;
C、同是s能级,在不同的能层中所能容纳的最多电子数是相同的,都是2个;
D、根据泡利不相容原理:每个原子轨道上最多只能容纳 2个自旋状态相反的电子.
解答 解:A、各电子层最多容纳电子数2n2(n为电子层数),故A错误;
B、任一能层的能级总是从s能级开始,而且能级数等于该能层序数,故B正确;
C、同是s能级,在不同的能层中所能容纳的最多电子数是相同的,都是2个,故C错误;
D、1个原子轨道里最多只能容纳2个电子,但自旋方向相反,故D错误;
故选B.
点评 本题主要是考查学生对能层与能级概念、判断的熟悉了解程度,属于识记性知识的检验,记住即可.


 春雨教育同步作文系列答案
春雨教育同步作文系列答案科目:高中化学 来源: 题型:解答题
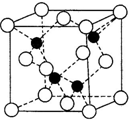 已知A、B、C、D、E、F都是元素周期表中前四周期的元素,它们的核电荷数依次递增.B原子的P轨道半充满,形成氢化物的沸点是同主族元素的氢化物中最低的.D原子得到一个电子后3P轨道全充满.A+比D原子形成的离子少一个电子层.C与A形成A2C型离子化合物.E的原子序数为31,F与B属同一主族,E与F形成的化合物常用于制造半导体.根据以上信息,回答下列问题:
已知A、B、C、D、E、F都是元素周期表中前四周期的元素,它们的核电荷数依次递增.B原子的P轨道半充满,形成氢化物的沸点是同主族元素的氢化物中最低的.D原子得到一个电子后3P轨道全充满.A+比D原子形成的离子少一个电子层.C与A形成A2C型离子化合物.E的原子序数为31,F与B属同一主族,E与F形成的化合物常用于制造半导体.根据以上信息,回答下列问题:查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 该反应为吸热反应 | B. | CO2的分子模型示意图: | ||
| C. | HCHO分子中既含σ键又含π键 | D. | 每生成1.8 g H2O消耗2.24 L O2 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 等于90% | B. | 大于90% | C. | 小于90% | D. | 无法判断 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 物质 | Cl2 | Br2 | I2 | HCl | HBr | HI | H2 |
| 能量(kJ) | 243 | 193 | 151 | 432 | 366 | 298 | 436 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | W与R形成的化合物只能含离子键 | |
| B. | M、X与R的最高价氧化物的水化物所组成的原电池中M作负极 | |
| C. | 简单气态氢化物的沸点:Y<W | |
| D. | 化合物Y2Z2中只含极性共价键 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
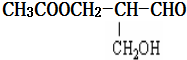
| A. | 与甲酸发生酯化反应 | B. | 与NaOH水溶液共热 | ||
| C. | 在铜作催化剂与氧气加热反应 | D. | 在催化剂存在下与氢气反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 正反应活化能小于100 kJ•mol-1 | |
| B. | 逆反应活化能一定小于100 kJ•mol-1 | |
| C. | 正反应活化能不小于100 kJ•mol-1 | |
| D. | 正反应活化能比逆反应活化能小100 kJ•mol-1 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com