
| ||
| ||
| 168g×0.62g |
| 62g |
| 106g×0.62g |
| 62g |
| 106×0.88g |
| 44 |
| 2mol×1.06g |
| 106g |
| 1mol×1.68g |
| 84g |


科目:高中化学 来源: 题型:
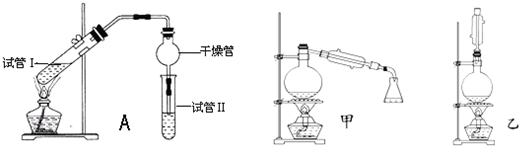
| 实验编号 | 试管Ⅰ中试剂 | 试管Ⅱ中试剂 | 有机层的厚度/cm |
| A | 2mL乙醇、1mL乙酸、 1mL 18mol?L-1浓硫酸 | 饱和Na2CO3溶液 | 3.0 |
| B | 2mL乙醇、1mL乙酸 | 0.1 | |
| C | 2mL乙醇、1mL乙酸、 3mL 2mol?L-1 H2SO4 | 0.6 | |
| D | 2mL乙醇、1mL乙酸、盐酸 | 0.6 |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、24克镁单质变为镁离子时,失去的电子数为NA |
| B、18克水所含的电子数为NA |
| C、8克氦气所含分子数为NA |
| D、3.2克氧气所含氧原子数为0.2NA |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、电解池的阴极上都是发生失电子的氧化反应 |
| B、用惰性电极电解Na2SO4溶液,阴、阳两极产物的物质的量之比为1:2 |
| C、用惰性电极电解饱和NaCl溶液,若有1 mol电子转移,则生成1molNaOH |
| D、酸、碱、盐溶液电解后pH都增大 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com