
【题目】短周期元素X、Y、Z、Q、W、R的原子序数与其常见化合价关系如下图所示。下列说法正确的是
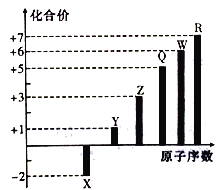
A. X、Y、R形成的某种化合物可以用于漂白、消毒
B. Q元素形成的可溶性盐的溶液不可能显酸性
C. X、Y、Z、W、R的简单离子半径大小顺序为R>W>Z>Y>X
D. Y、Z和W三者最高价氧化物对应的水化物间不能两两相互反应
 优学名师名题系列答案
优学名师名题系列答案科目:高中化学 来源: 题型:
【题目】阅读下列信息: Ⅰ.表中①~⑥为短周期元素主要化合价及最简单氢化物沸点的数据:
元素性质 | 元素编号 | |||||
① | ② | ③ | ④ | ⑤ | ⑥ | |
氢化物沸点(℃) | ﹣33.4 | 100 | 19.54 | ﹣87.7 | ﹣60.7 | ﹣84.9 |
主要化合价 | +5 | ﹣2 | ﹣1 | +5 | +6 | +7 |
A、B、C均为上表中的元素;
Ⅱ.A与B可形成化合物AB、AB2 , 二者可用于制备强酸甲;
Ⅲ.C与B可形成化合物CB2、CB3 , 二者可用于制备强酸乙.
请回答:
(1)该表中两种元素的氢化物所含电子数不同,这两种氢化物之间能发生反应,写出符合要求的化学方程式(有多组符合,写出任意一个即可).
(2)元素②氢化物的沸点高于元素⑤氢化物的沸点,原因是 .
(3)甲、乙分别与氨反应生成丙、丁、戊三种盐.0.1mol/L的甲、乙、丙、丁、戊五种溶液,pH由小到大排列的顺序是(填写化学式) .
(4)很稀的甲溶液与Zn反应,当反应的甲与Zn的物质的量之比为5:2时,还原产物可能为(填写化学式)、 .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某有机物的结构为下图所示,这种有机物不可能具有的性质是( ) ①可以燃烧;②能使酸性KMnO4溶液褪色;
③能跟NaOH溶液反应; ④能发生酯化反应;
⑤能发生加聚反应;⑥能发生水解反应.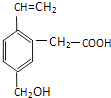
A.①④
B.只有⑥
C.只有⑤
D.④⑥
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】以NA代表阿伏加德罗常数的值,下列说法正确的是
A. 标准状况下,22.4LHF中含有的氟原子数目为NA
B. 12g石墨烯(单层石墨)中含有的六元环个数为NA
C. 标准状况下,6.0gNO和2.24LO2混合,所得气体的分子数目为0.2NA
D. 反应N2(g)+3H2(g)![]() 2NH3(g) △H=-92.4kJ/mol,若放出热量4.62kJ,则转移的电子数目为0.3NA
2NH3(g) △H=-92.4kJ/mol,若放出热量4.62kJ,则转移的电子数目为0.3NA
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某烃有两种或两种以上的同分异构体,其某一种同分异构体的一氯代物只有一种,则这种烃可能是( ) ①分子中含有7个碳原子的芳香烃 ②分子中含有4个碳原子的烷烃
③分子中含有12个氢原子的烷烃 ④分子中含有8个碳原子的烷烃.
A.③④
B.②③
C.①②
D.②④
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下图虚线框中的装置(试剂均足量)可用来检验浓硫酸与木炭粉在加热条件下反应所产生的所有气体产物,下列说法正确的是
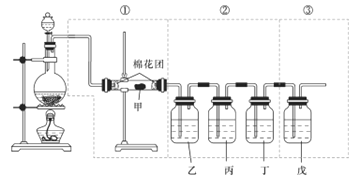
A. 物质甲可以是无水硫酸铜、变色硅胶、无水氯化钙等物质
B. 丙中发生反应的离子方程式可能是SO2+2OH-=SO32-+H2O
C. 乙和戊两种溶液都不宜用作尾气吸收装置中的试剂
D. 如果将装置的连接顺序变为①③②,则只能检验出两种产物
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】同周期的X、Y和Z三种元素,已知H3ZO4、H2YO4和HXO4的酸性依次增强,下列判断不正确的是( )
A.非金属性:X最强,Z最弱
B.气态氢化物稳定性:HX最强
C.X可能是氟元素
D.原子半径:Z最大,X最小
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】现有一定量的镁铝合金与100 mL 稀硝酸充分反应,在反应过程中无气体放出。在反应结束后的溶液中,逐滴加入1.00mol/ L NaOH溶液,加入NaOH 溶液的体积与产生沉淀的物质的量关系如图所示:
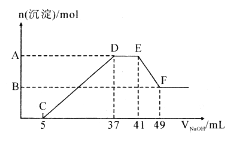
(1)合金中的铝与稀硝酸反应的化学方程式为_________;
(2)纵坐标上A 点数值是__________,B 点数值是_________;
(3)原HNO3 溶掖的物质的量浓度为_________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法不正确的是( )
A. 用氯气制漂白粉的主要目的是转变为较稳定,便于贮存的物质
B. 漂白粉在空气中容易失效的原因是次氯酸钙易和空气中的水及二氧化碳反应
C. 氯原子最外层有 7 个电子,故在化学反应中易结合一个电子而形成 Cl﹣
D. 次氯酸是一种弱酸是因为次氯酸不稳定,易分解
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com