
 如图是用0.1000mol/L的盐酸滴定某未知浓度的NaOH溶液的示意图和某次滴定前、后的盛放盐酸滴定管中液面的位置.请回答:
如图是用0.1000mol/L的盐酸滴定某未知浓度的NaOH溶液的示意图和某次滴定前、后的盛放盐酸滴定管中液面的位置.请回答:| 实验 编号 | 待测NaOH溶液的体积(mL) | 滴定前盐酸的 体积读数(mL) | 滴定后盐酸的 体积读数(mL) |
| 1 | 20.00 | 1.20 | 23.22 |
| 2 | 20.00 | 2.21 | 24.21 |
| 3 | 20.00 | 1.50 | 23.48 |
分析 (1)根据仪器的结构来分析;
(2)根据滴定管的结构与精确度为0.01mL;
(3)先根据数据的有效性,然后求出平均消耗V(NaOH),根据c(待测)=$\frac{c(标注)×V(标准)}{V(待测)}$计算;
(4)根据溶液颜色变化且半分钟内不变色,可说明达到滴定终点;
(5)根据c(待测)=$\frac{c(标注)×V(标准)}{V(待测)}$来判断不当操作对相关物理量的影响.
解答 解:(1)该滴定管的下端是玻璃活塞,所以仪器的名称为酸式滴定管,
故答案为:酸式滴定管;
(2)滴定前,滴定管中的液面读数为0.80mL,滴定后,滴定管中的液面读数为22.80mL,
故答案为:0.80;22.80;
(3)三次滴定消耗的体积为:22.02mL,22.00mL,21.98mL,数据均有效,则平均消耗V(NaOH)=22.00mL,c(待测)=$\frac{c(标注)×V(标准)}{V(待测)}$=
$\frac{0.1000mol/L×22.00mL}{20.00mL}$=0.1100mol•L-1,
故答案为:0.1100;
(4)滴定时,当溶液颜色由粉红色变为无色,且半分钟内不变色,可说明达到滴定终点,
故答案为:当溶液颜色由粉红色变为无色,且半分钟内不变色;
(5)①若滴定前锥形瓶未用待测液润洗,待测液的物质的量不变,标准液的体积也不变,根据c(待测)=$\frac{c(标注)×V(标准)}{V(待测)}$分析,测定结果无影响;
②取待测液的滴定管,滴定前滴定管尖端有气泡,滴定后气泡消失,导致标准液的体积偏大,根据c(待测)=$\frac{c(标注)×V(标准)}{V(待测)}$分析,测定结果偏高;
③标准液读数时,若滴定前仰视,滴定后俯视,导致标准液的体积偏小,根据c(待测)=$\frac{c(标注)×V(标准)}{V(待测)}$分析,测定结果偏低;
故答案为:无影响;偏高;偏低.
点评 本题考查酸碱中和滴定,明确中和滴定实验的仪器、步骤、终点的判定、数据处理等即可解答,注意滴定管的读数为易错点.


科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
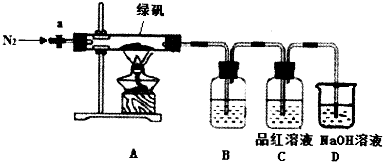
 草酸亚铁晶体(FeC2O4•2H2O)呈淡黄色.某课题组为探究草酸亚铁晶体的化学性质,进行了一系列实验探究.
草酸亚铁晶体(FeC2O4•2H2O)呈淡黄色.某课题组为探究草酸亚铁晶体的化学性质,进行了一系列实验探究.| 实验步骤(不要求写出具体操作过程) | 预期实验现象和结论 |
| 取少量黑色固体,加入适量稀盐酸或稀硫酸, 在溶液中加入硫氰化钾溶液 | 溶液不变红色,则假设一成立, 溶液变成红色,则假设一不成立 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 单质的沸点:e>d | |
| B. | 原子半径:r(e)>r(d) | |
| C. | 最高价氧化物对应水化物的酸性:c<d | |
| D. | a、b可以形成离子化合物 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| 实验编号 | 温度/℃ | 平衡常数/mol-1•L | 起始量/mol | 平衡量/mol | 达到平衡所需时间/min | ||
| SO2 | O2 | SO2 | O2 | ||||
| 1 | T1 | K1 | 4 | 2 | x | 0.8 | 6 |
| 2 | T2 | K2 | 4 | 2 | 0.4 | y | t |
| A. | x=1.6,y=0.2,t<6 | |
| B. | T1、T2的关系:T1>T2 | |
| C. | K1、K2的关系:K2>K1 | |
| D. | 实验1在前6 min的反应速率v (SO2)=0.2 mol•L-1•min-1 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | C0和H2混合物lmol.完全燃烧消耗O2的分子数为0.5NA | |
| B. | lmolCnH2n+2 所含的共用电子对数为(3n+l)NA | |
| C. | 标准状况下,22.4L甲醇所含的分子数目为NA | |
| D. | 高温下,33.6g Fe与足量水蒸气反应,生成的H2分子数目为0.8NA |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 ,D原子的价层电子排布式为3s23p3.
,D原子的价层电子排布式为3s23p3.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
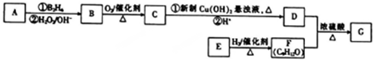
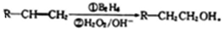
 .
. (填结构简式).
(填结构简式).查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com