
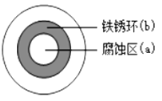
【题目】将 NaCl 溶液滴在一块光亮清洁的铁板表面上,一段时间后发现液滴覆盖的圆周中心区(a)已被腐蚀而变暗,在液滴外沿棕色铁锈环(b),如图所示。下列说法不正确的是( )
A. 铁片腐蚀过程发生的总化学方程式为:4Fe+6H2O+3O2 ==4 Fe(OH)3
B. 液滴之下氧气含量少, 铁片作负极,发生的还原反应为: Fe-2e-=Fe2+
C. 液滴边缘是正极区,发生的电极反应为: O2+2H2O+4e-=4OH-
D. 铁片腐蚀最严重区域不是生锈最多的区域
【答案】B
【解析】
NaCl溶液滴到一块光亮清洁的铁板表面上,一段时间后在液滴覆盖的圆周中心区(a)被腐蚀变暗,实际上是发生了吸氧腐蚀,铁片作负极,发生的氧化反应,电极反应为:Fe-2e-=Fe2+,液滴边缘是正极区,电极反应为:O2+2H2O+4e-=4OH- (发生还原反应),在液滴外沿,由于Fe2++2OH-=Fe(OH)2,4Fe(OH)2+O2+2H2O=4Fe(OH)3 形成了棕色铁锈环(b),铁片腐蚀过程发生的总化学方程式为:4Fe+6H2O+3O2═4 Fe(OH)3,据此分析解答。
A.根据以上分析,铁片腐蚀过程发生的总化学方程式为:4Fe+6H2O+3O2═4 Fe(OH)3,故A正确;B.铁片作负极,发生的氧化反应,电极反应为:Fe-2e-=Fe2+,故B错误;C.O2在液滴外沿反应,正极电极反应为:O2+2H2O+4e-=4OH- (发生还原反应),故C正确。D.铁片腐蚀最严重区域不是生锈最多的区域,而是液滴中心区,故D正确;故答案为B。


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
【题目】对三联苯是一种有机合成中间体,工业上合成对三联苯的化学方程式为:![]() +2H2↑。下列说法正确的是( )
+2H2↑。下列说法正确的是( )
A. 三联苯不是苯的同系物 B. 对三联苯分子中至少有14个碳原子共平面
C. 对三联苯的一氯取代物有3种 D. 对三联苯的分子式为C18Hl8
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有机物X、Y、Z的分子式均为C7H8,结构简式如下:

下列说法正确的是( )
A. X、Y、Z均为苯的同系物
B. X、Y、Z分子中的碳原子均处于同一平面
C. X、Y、Z均能使酸性高锰酸钾溶液褪色
D. 1molX、1molY分别与足量溴的四氯化碳溶液反应,均最多消耗2mol Br2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】A~I分别表示中学化学中常见的一种物质,其中A、I为常见金属,它们之间的相互关系如图所示(部分反应物、生成物没有列出),且已知G为主族元素的固态氧化物,A、B、C、D、E、F六种物质中均含同一种元素。请填写下列空白:

(1)A、B、C、D、E、F六种物质中所含同一种元素在周期表中的位置是________。
(2)写出C物质的化学式:________。
(3)写出下列反应的化学方程式或离子方程式:
反应①的化学方程式:____________________________;
反应④的离子方程式:____________________________;
反应⑥的化学方程式:____________________________。
(4)从能量变化的角度看,反应①②③中,属于ΔH<0的反应是________(填序号)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】类比pH的定义,对于稀溶液可以定义pC=-lgC,pKa=-lgKa。常温下,某浓度H2A溶液在不同pH值下,测得pC(H2A)、pC(HA-)、pC(A2-)变化如图所示。下列说法正确的是
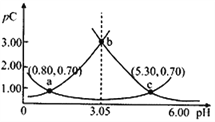
A. pH=3.50时,c(H2A)>c(HA-)>c(A2-)
B. 常温下,pKa1(H2A)=5.30,pKa2(H2A)=0.80
C. b点时,![]() =104.50
=104.50
D. pH=3.00~5.30时,c(H2A)+c(HA-)+c(A2-)先增大后减小
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】2SO2(g)+O2(g)![]() 2SO3(g)反应过程中的能量变化如图所示(图中E1表示无催化剂时正反应的活化能,E2表示无催化剂时逆反应的活化能)。下列有关叙述不正确的是
2SO3(g)反应过程中的能量变化如图所示(图中E1表示无催化剂时正反应的活化能,E2表示无催化剂时逆反应的活化能)。下列有关叙述不正确的是

A. 该反应的逆反应为吸热反应,升高温度可提高活化分子的百分数
B. 500℃、101kPa下,将1molSO2(g)和0.5molO2(g)置于密闭容器中充分反应生成SO3(g)放热akJ,其热化学方程式为2SO2(g)+O2(g)![]() 2SO3(g) ΔH=-2a kJ·mol-l
2SO3(g) ΔH=-2a kJ·mol-l
C. 该反应中,反应物的总键能小于生成物的总键能
D. ΔH=E1-E2,使用催化剂改变活化能,但不改变反应热
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)工业上用_______和_______为原料制取漂白粉,有效成份是_______,制备原理是______________________(方程式表示)。漂白粉用于漂白的时候,最好与稀盐酸反应,有关化学方程式为______________________________________。
(2)Ca元素在周期表中的位置是__,Ca与最活泼的非金属元素A形成化合物D,D的电子式为___,HCl的沸点比A与H形成的化合物HA的沸点__(填“高”或“低”)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列图示中,A是一种常见的单质,B、C、D、E是含A元素的常见化合物,它们的焰色反应的火焰均呈黄色。

填写下列空白:
(1)写出化学式:A_____,B_____,D______________。
(2)以上反应中属于氧化还原反应的有_____(填序号)。
(3)写出反应⑤的离子方程式:___。写出反应⑥的化学方程式:___。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com