
科目:高中化学 来源:专项题 题型:填空题
 CH3COO-+H+ ; △H>0
CH3COO-+H+ ; △H>0查看答案和解析>>
科目:高中化学 来源:模拟题 题型:填空题
研究化学反应原理对于生产生活是很有意义的。
(1)25℃时,醋酸溶液中CH3COOH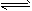 CH3COO-+ H+;Ka= 1.75×10-5 mol/L,若向0.10 mol/LCH3COOH溶 液中加入一定量的固体CH3COONa(假设溶液体积不变),若溶液中c(CH3COO-)为1.0 mol/L,则溶液中c(H+)=_______mol/L(计算结果保留小数点后两位数字)。溶液中各种离子浓度关系是__________。
CH3COO-+ H+;Ka= 1.75×10-5 mol/L,若向0.10 mol/LCH3COOH溶 液中加入一定量的固体CH3COONa(假设溶液体积不变),若溶液中c(CH3COO-)为1.0 mol/L,则溶液中c(H+)=_______mol/L(计算结果保留小数点后两位数字)。溶液中各种离子浓度关系是__________。
(2)牙釉质对牙齿起着保护作用,其主要成分为Ca5(PO4)3OH,该物质在水中存在沉淀溶解平衡,试写出该物质的溶度积常数表达式Ksp=_____________。
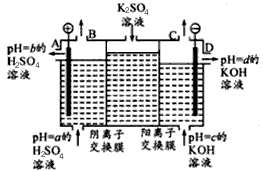
(3)某小组运用工业上离子交换膜法制烧碱的原理,用如下图所示装置电解K2SO4溶液。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com