
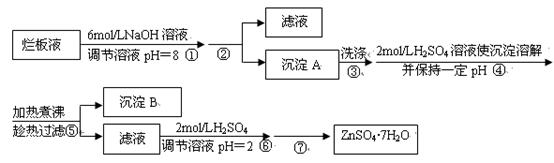
| 离子 | 开始沉淀时的pH | 完全沉淀时的pH |
| Fe3+ | 1.9 | 3.2 |
| Zn2+ | 6.4 | 8.0 |
科目:高中化学 来源:不详 题型:单选题
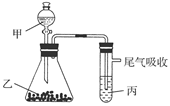
| | 甲 | 乙 | 丙 | 结论 |
| A | 水 | 电石 | 溴水 | 稳定性:水>C2H2>Br2 |
| B | 盐酸 | 石灰石 | 苯酚钠溶液 | 酸性:HCl>H2CO3>苯酚 |
| C | 盐酸 | FeS | 溴水 | 还原性:S2->Br->Cl- |
| D | 浓盐酸 | KMnO4 | KBr溶液 | 氧化性:KMnO4<Cl2<Br2 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
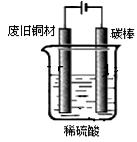
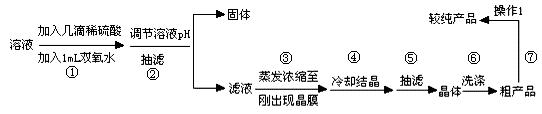
| 离子 | 开始沉淀的pH | 完全沉淀的pH |
| Fe2+ | 6.4 | 8.4 |
| Fe3+ | 2.4 | 3.1 |
| Cu2+ | 5.2 | 6.5 |
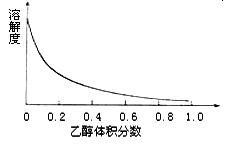
| A.无水乙醇 | B.蒸馏水 |
| C.95%乙醇溶液 | D.饱和硫酸钠溶液 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:实验题

查看答案和解析>>
科目:高中化学 来源:不详 题型:实验题

查看答案和解析>>
科目:高中化学 来源:不详 题型:实验题
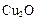 可作为太阳光分解水的催化剂。
可作为太阳光分解水的催化剂。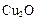 的方法
的方法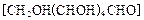 还原新制的
还原新制的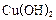 。写出化学方程式 ;
。写出化学方程式 ;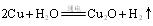 。则阳极产物是 ;
。则阳极产物是 ;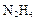 )还原新制
)还原新制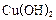 可制备纳米级
可制备纳米级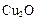 ,同时放出
,同时放出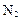 。该制法的化学方程式为 。
。该制法的化学方程式为 。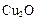 进行催化分解水的实验
进行催化分解水的实验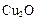 并通入0.10mol水蒸气,发生反应:
并通入0.10mol水蒸气,发生反应: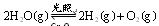 ;△H= +484kJ/mol,不同时段产生
;△H= +484kJ/mol,不同时段产生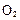 的量见下表:
的量见下表:| 时间/min | 20 | 40 | 60 | 80 |
| n(O2)/mol | 0.0010 | 0.0016 | 0.0020 | 0.0020 |
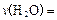 ;达平衡时,至少需要吸收的光能为 kJ。
;达平衡时,至少需要吸收的光能为 kJ。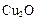 在某相同条件下分别对水催化分解,产生氢气的速率v随时间t变化如图所示。下列叙述正确的是 。
在某相同条件下分别对水催化分解,产生氢气的速率v随时间t变化如图所示。下列叙述正确的是 。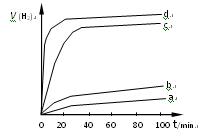
A.c、d方法制得的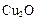 催化效率相对较高 催化效率相对较高 |
B.d方法制得的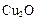 作催化剂时,水的平衡转化率最高 作催化剂时,水的平衡转化率最高 |
C.催化效果与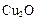 颗粒的粗细、表面活性等有关 颗粒的粗细、表面活性等有关 |
| D.Cu2O催化水分解时,需要适宜的温度 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:实验题
 CO↑ + CO2↑ + H2O,下列装置中,可用作草酸分解制取气体的是 ▲ 。(填字母)
CO↑ + CO2↑ + H2O,下列装置中,可用作草酸分解制取气体的是 ▲ 。(填字母)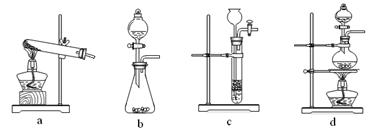
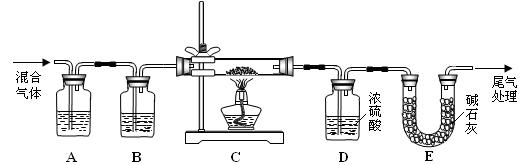
 进行的操作是:(a)检查装置气密性;(b) ▲ 。
进行的操作是:(a)检查装置气密性;(b) ▲ 。查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
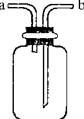
| A.干燥CO2:瓶内放一定体积浓硫酸,由a进气 |
| B.用于收集O2:瓶内充满水,由b进气 |
| C.提供少量CO:瓶内充满CO,b接进水管 |
| D.用做H2S和SO2反应的装置:由a通入H2S,b通入SO2 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com