
����Ŀ��������ˮ�п��ܴ��ڵ���ƽ�⡢�ε�ˮ��ƽ��ͳ������ܽ�ƽ�⣬���Ƕ��ɿ�����ѧƽ�⣮
�������ѧ֪ʶ�Ļش�
��1��Ũ��Ϊ0.1mol/L��8����Һ����HNO3 ��H2SO4��HCOOH ��Ba��OH��2��NaOH ��CH3COONa ��KCl ��NH4Cl ��ҺpHֵ��С�����˳���ǣ���д��ţ� ��
��2��BΪ0.1molL��1NaHCO3��Һ��ʵ����NaHCO3��Һ��pH��7���������ӷ���ʽ��ʾ��ԭ�� ��
��3����0.10molL��1����ͭ��Һ�м�����������ϡ��Һ��ֽ�����dz��ɫ������ͭ�������ɣ�����Һ��pH=8ʱ��c��Cu2+��=����֪Ksp[Cu��OH��2]=2.2x10��20��������0.10molL��1����ͭ��Һ��ͨ�����H2S���壬ʹCu2+��ȫ����ΪCuS����ʱ��Һ�е�H+Ũ���ǣ�
���𰸡�
��1���ڢ٢ۢ�ߢޢݢ�
��2��HCO3+H2O?H2CO3+OH��
��3��2.2��10��8mol?L��1
���������⣺��1�����ڼ��Ϊ����Ba��OH��2��NaOH��Ũ����ͬʱ�����Ԣܣ��ݣ�ˮ��ʼ��Ե�Ϊ����CH3COONa����ˮ��̶Ƚ�С����pH���ܣ��ݣ��ޣ�
��Һ�����Ե�Ϊ����KCl��
��Һ�����Ե��У��٢ڢۢ࣬���Т�ΪһԪǿ�ᣬ��Ϊ��Ԫǿ�ᣬ��Ϊ���ᣬ��ˮ������ԣ�Ũ����ͬʱ��
��Һ��pH���ڣ��٣��ۣ��࣬
�ۺ����Ϸ�����֪����Һ��pH��С�����˳����Ϊ���ڢ٢ۢ�ߢޢݢܣ�
���Դ��ǣ��ڢ٢ۢ�ߢޢݢܣ���2����NaHCO3��Һ�д���̼��������ӵ�ˮ��ƽ��Ϊ��HCO3+H2OH2CO3+OH�� �� ����ƽ��Ϊ��HCO3��H++CO32�� �� ����ˮ��Ϊ������̼��������ӵ�ˮ��̶ȴ��ڵ���̶���Һ�����Լ��ԣ�
���Դ��ǣ�HCO3+H2OH2CO3+OH������3���������Cu��OH��2���ܶȻ�����ȷ��pH=8ʱ��c��OH����=10��6mol/L��Ksp[Cu��OH��2]=2.2��10��20 �� ��c��Cu2+��= ![]() =2.2��10��8molL��1��
=2.2��10��8molL��1��
��0.1molL��1����ͭ��Һ��ͨ�����H2S���壬ʹCu2+��ȫ����ΪCuS����ʱ��Һ�е�����Ϊ���ᣬc��SO42�������䣬Ϊ0.1molL��1 �� �ɵ���غ��֪c��H+��Ϊ0.2molL��1 ��
���Դ��ǣ�2.2��10��8molL��1��0.2molL��1 ��


 ��У����ϵ�д�
��У����ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��Ϊ̽��Cl2��Br2��Fe3+��������ǿ����ij��ѧ��ȤС�����������ʵ����

��1����A����������װ�����䷴Ӧ�����ӷ���ʽ��__________________________________��
��Bװ�õ�������_________________________��Cװ�õ�������_______________________������ʵ��װ�ô���һ�����Բ��㣬��ָ��_______________________________________________________��
��2���ø������װ�ý���ʵ�顣ʵ��������£�
ʵ����� | ʵ������ |
����a����Բ����ƿ�е�������Ũ���ᣬȻ��رջ���a����ȼ�ƾ��� | Dװ���У���Һ��� Eװ���У� ��ˮ����Һ��ƣ�CCl4�����Ա仯 |
��������Ũ���ᣬD��E�о��������µı仯��
Dװ���У���ɫ������ȥ��Eװ���У�CC14��������ɫ��Ϊ��ɫ������ɫ��ɺ�ɫ��
Ϊ̽������ʵ������ı��ʣ�С��ͬѧ����������£�
I��(SCN)2 ������±�����ƣ�������Cl2����(SCN)2����SCN-�ĵ���ʽΪ![]()
II��AgClO��AgBrO ��������ˮ
����Cl2 ��Br2��Ӧ����BrCl��BrCl�ʺ�ɫ���е�ԼΪ5������ˮ����ˮ�ⷴӦ
��С��ͬѧ��ΪDװ���к�ɫ��ȥ��ԭ��������SCN-��Cl2��������һ������̼Ԫ�ر�����������������__________________________________________��
������ʵ��֤ʵ��С��ͬѧ�Ʋ�ĺ����ԣ�����ƽ���ƶ�ԭ������Cl2����ʱD����Һ��ɫ��ȥ��ԭ��__________________________________________��
����̽��E �м����μ�Ũ�������ɫ�仯��ԭ�����ʵ���������÷�Һ©�������E���²���Һ�������ռ���ɫ���ʣ�ȡ����������AgNO3��Һ������۲쵽���а�ɫ�������������ϻ�ѧ������ͽ�������ɫ������ԭ��_________________________________________________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����ѧƽ�ⳣ�������� K ����ʾ�����й��� K ��˵������ȷ���ǣ�������
A.K Խ��Ӧ���ת����ԽС
B.K ���¶�һ���й�
C.K ���������Ũ��һ���й�
D.K �뷴Ӧ���Ũ��һ���й�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��������Һ��������������ʢ�ţ�����Ϊ���������е�����ͭ��Ӧ���ڸ÷�Ӧ������ͭ��
A. ��ԭ�� B. ������ C. ���� D. �����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������������ԭ��Ӧ��2Ag+��aq��+Cu��s���TCu2+��aq��+2Ag��s����Ƶ�ԭ�����ͼ��ʾ����ش��������⣺ 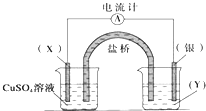
��1���缫X�IJ����� �� �������ҺY����
��2�����缫Ϊ��ص����������ĵ缫��ӦΪX�缫�Ϸ����ĵ缫��ӦΪ ��
��3�����·�еĵ����Ǵ��缫�����缫��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����25��ʱ������0.1molL��1�İ�ˮ����ش��������⣺
��1������ˮ�м�����������粒��壬��ʱ��Һ�� ![]() �������������С�����䡱����
�������������С�����䡱����
��2������ˮ�м���pH=1�����ᣬ�Ұ�ˮ������������Ϊ1��1����ʱ��Һ��pH7������ڡ�����С�ڡ����ڡ����������ӷ���ʽ��ʾ��ԭ�� �� ��ʱ��Һ�и�����Ũ���ɴ�С��˳��Ϊ ��
��3������ˮ�м���0.05molL��1ϡ��������Һ���ó����ԣ����ð�ˮ�����V1��ϡ��������V2�Ĺ�ϵΪV1V2������ڡ�����С�ڡ����ڡ�����д����Һ�и�����Ũ��֮������ĵ���غ����ʽ ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������˵����ȷ���ǣ�������
A.Ϊ��������͵IJ���������ʯ�ͽ��м�ѹ����
B.ͨ��ʯ�͵ķ�������Ƶ���ϩ
C.ú�к��б����ױ��ȣ�ͨ��ú�ĸ���ɵõ�������
D.ú�����л����������ɵĸ��ӵĻ����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����һ��������Mg��Al�����Ͷ�뵽200mLϡ�����У�����ȫ���ܽ����������Һ�еμ�NaOH��Һ�����������ɳ��������ʵ��������NaOH��Һ�������ϵ��ͼ��ʾ��������˵������ȷ���ǣ� ��
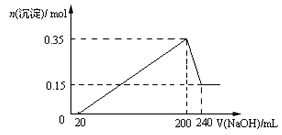
A. Mg��Al��������Ϊ9g
B. ���20mLNaOH��Һ�����к�����ϡ����
C. NaOH��Һ���ʵ���Ũ��Ϊ5mol��L-1
D. ���ɵ������ڱ�״���µ����Ϊ11.2L
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����з�Ӧ��CO��g��+H2O��g��CO2��g��+H2��g����H��0����850��ʱ��ƽ�ⳣ��K=1������850��ʱ����2L���ܱ������г���CO��H2O��g����4mol���Իش��������⣨д������ļ�����̣���
��1����ƽ��ʱ��COת����Ϊ���٣�
��2��H2���������Ϊ���٣�
��3�����¶���Ϊ850�棬��ʼʱCOŨ��Ϊ2mol/L��H2O��g��Ϊ6mol/L����ƽ��ʱCOת����Ϊ���٣�
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com