
| A、同一主族元素的原子,最外层电子数相同,化学性质完全相同 |
| B、同主族元素含氧酸性随核电核数的增加而减弱 |
| C、元素周期表是元素原子核外电子排布周期性变化的结果 |
| D、非金属元素形成的共价化合物中,原子的外层电子数只能是2或8 |


科目:高中化学 来源: 题型:
| A、同温同压下,相同体积的物质,它们的物质的量必相同 |
| B、常温常压下,等质量的N2与CO所含分子数相同 |
| C、V L O2的质量一定比V L CO2的质量小 |
| D、A容器中的H2与B容器中的NH3所含原子总数相等,由两容器的体积比为2:1 |
查看答案和解析>>
科目:高中化学 来源: 题型:

| HCN/OH- |

| H2O/H+ |

 ,该物质在NaOH水溶液中加热反应时的化学方程式为
,该物质在NaOH水溶液中加热反应时的化学方程式为 的合成路线流程图(无机试剂任用).
的合成路线流程图(无机试剂任用).| HBr |
| NaOH溶液 |
| △ |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、除去乙烷中混有的少量乙烯:通入溴水,干燥 |
| B、除去溴苯中混有的少量单质溴:加入足量的NaOH溶液,振荡、静置、分液 |
| C、除去96%的乙醇中的少量水制无水乙醇:加入生石灰,振荡、静置、蒸馏 |
| D、除去乙醇中的微量水可加入金属钠,使其完全反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:

| 烃 | CH4 | CH3CH3 | CH3(CH2)2CH3 | 硝基苯酚 |  |  | 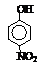 |
| 沸点/℃ | -164 | -88.6 | -0.5 | 熔点/℃ | 45 | 96 | 114 |
查看答案和解析>>
科目:高中化学 来源: 题型:
 25℃时,向盛有50mL pH=2的HA溶液的绝热容器中加入pH=13的NaOH溶液,加入NaOH溶液的体积(V)与所得混合溶液的温度(T)的关系如图所示.下列叙述正确的是( )
25℃时,向盛有50mL pH=2的HA溶液的绝热容器中加入pH=13的NaOH溶液,加入NaOH溶液的体积(V)与所得混合溶液的温度(T)的关系如图所示.下列叙述正确的是( )| A、HA溶液的物质的量浓度为0 0l mol.L-1 |
| B、b→c的过程中,温度降低的原因是溶液中发生了吸热反应 |
| C、a→b的过程中,混合溶液中可能存在:c(A-)=c(Na+) |
| D、25℃时,HA的电离平衡常数K约为1.43×10-2 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、标准状况下,将22.4 L氯化氢溶于足量水中,溶液中含有的HCl分子数为NA |
| B、常温常压下,16 g 14CH4所含中子数目为8NA |
| C、常温常压下,Na2O2与足量H2O反应,共生成0.2 mol O2,转移电子的数目为0.4 NA |
| D、标准状况下,22.4 L空气含有NA个单质分子 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| 选项 | 实验操作 | 现象 | 结论 | ||
| A | ①向溶液中通入CO2②继续通入CO2浑浊至过量 | ①溶液变浑浊②浑浊不消失 | 原溶液一定是NaAlO2溶液 | ||
| B | ①想溶液中加入KSCN溶液②滴入一定量盐酸 | ①溶液无明显现象②溶液变为血红色 | 原溶液中可能含有Fe2+NO
| ||
| C | 用洁净帕丝蘸取少量溶液进行焰色反应 | 火焰呈黄色 | 原溶液一定是钠盐溶液 | ||
| D | 溶液中加入盐酸 | 产生的气体使澄清石灰水变浑浊 | 原溶液中一定含有CO
|
| A、A | B、B | C、C | D、D |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com