
已知煤的部分结构模型如图所示:
(1)从煤的结构模型来看,煤是工业上获得 烃的重要来源。
(2)我国大约70%的煤是直接用于燃烧的。从煤的结构模型来看,在提供热量的同时产生大量的 等气体物质,造成严重的大气污染。
(3)“型煤”技术不仅可以减少87%的废气排放量,烟尘排放量也可减少80%,致癌物苯并[a]芘的排放量也减少,同时节煤20%~30%。“型煤”技术的原理是利用固硫剂在燃烧过程中生成稳定的硫酸盐。下列物质中适宜于作固硫剂的是 (填字母)。
A.氯化钙 B.氧化钙
C.硫酸钙 D.氢氧化钙
(4)某“型煤”生产厂利用石灰石作固硫剂,试用化学方程式表示其“固硫”过程___________________________________________________。
(5)除上述的“型煤”技术外,为了解决煤燃烧所造成的污染问题和提高煤的利用价值,煤资源的综合利用方法还有 、 、 等。
科目:高中化学 来源: 题型:
下列叙述正确的是( )
A.Fe与稀HNO3、稀H2SO4反应均有气泡产生,说明Fe与两种酸均发生置换反应
B.足量的Fe在Cl2中燃烧生成FeCl2和FeCl3
C.Fe和Fe2O3等物质的量混合物溶于稀盐酸时无气体放出
D.Fe2O3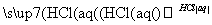 FeCl3(aq)
FeCl3(aq)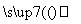 无水FeCl3,在给定的条件下能实现转化
无水FeCl3,在给定的条件下能实现转化
查看答案和解析>>
科目:高中化学 来源: 题型:
氧化还原反应广泛应用于金属的冶炼。下列说法不正确的是( )
A.冶炼铁的主要原料有铁矿石、焦炭、空气、石灰石等,其中石灰石的作用是除去铁矿石中的脉石(二氧化硅)
B.湿法炼铜与火法炼铜的反应中,铜元素都发生还原反应
C.工业上Mg可由电解熔融的MgO制取,Na也可由电解熔融的NaCl制取
D.铝热法还原铁的反应中,放出的热量能使铁熔化
查看答案和解析>>
科目:高中化学 来源: 题型:
人体中的钙元素主要存在于骨骼和牙齿中,以羟基磷酸钙晶体[Ca10(PO4)6(OH)2]形式存在。牛奶含钙丰富又易吸收,且牛奶中钙和磷比例合适,是健骨的理想食品。下图是某乳业公司纯牛奶包装标签的部分文字。请仔细阅读后回答下列问题:
 纯牛奶
纯牛奶
配料:鲜牛奶
保质期:8个月
净含量:250 mL/盒
营养成分(每100 mL)
钙≥0.11 g
脂肪≥3.3 g
蛋白质≥2.9 g
(1)羟基磷酸钙中钙元素的质量分数______(保留1位小数)。
(2)包装标签上脂肪≥3.3 g,是指100 mL牛奶中含脂肪至少3.3 g。那么一盒牛奶中含钙至少________g(保留2位小数)。
查看答案和解析>>
科目:高中化学 来源: 题型:
将两个铂电极插入KOH溶液中,向两极分别通入CH4和O2,构成甲烷燃料电池。已知,通入CH4的一极,其电极反应式是:CH4+10OH--8e-===CO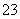 +7H2O;另一极通入O2。下列叙述不正确的是 ( )。
+7H2O;另一极通入O2。下列叙述不正确的是 ( )。
A.通入CH4的电极为负极
B.正极发生氧化反应
C.燃料电池工作时,溶液中的OH-向负极移动
D.该电池使用一段时间后应补充KOH
查看答案和解析>>
科目:高中化学 来源: 题型:
合成氨工业对国民经济和社会发展具有重要的意义。对于密闭容器中的反应:
|
 N2(g)+3H2(g) 2NH3(g),△H<0,
N2(g)+3H2(g) 2NH3(g),△H<0, 在673K、30Mpa下n(NH3)和n(H2)
随时间变化的关系如图所示。下列叙述
正确的是( )
A.点c处反应达到平衡
B.点a的正反应速率比点b的大
C.点d(t1时刻)和点e(t2时刻)处n(N2)不一样
D.其它条件不变,773K下反应至t1时刻,n(H2)比图中d点的值小
查看答案和解析>>
科目:高中化学 来源: 题型:
对于平衡体系mA(气)+nB(气) PC(气)十qD(气) △H <0,有下列判断,其中
正确的是 ( )
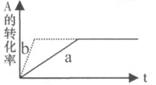 A.若温度不变,将容器的体积缩小1倍,此时A的浓度变为原来的1 .8倍,则m+n<p+q
A.若温度不变,将容器的体积缩小1倍,此时A的浓度变为原来的1 .8倍,则m+n<p+q
B.若平衡时,A、B的转化率相等,说明反应开始时A,B的物质的量之比为m:n
C.若平衡体系共有气体amol,再向其中加人bmolB,当重新达到平衡时,气体的总物质的量等于(a+b),则m+n>p+q
D.加催化剂或增大压强,可实现右图a→b的变化
查看答案和解析>>
科目:高中化学 来源: 题型:
判断,正确的划“√”,错误的划“×”
(1)用酸性高锰酸钾溶液鉴别苯、环己烯和环己烷( )
(2013·海南,7D)
(2)环戊烷( )在光照下与氯气反应,只生成一种一氯代物( )
)在光照下与氯气反应,只生成一种一氯代物( )
(2013·海南,9B改编)
(3)乙烯、聚氯乙烯和苯分子中均含有碳碳双键( )
(2013·福建理综,7C)
(4)丙烯的结构简式:C3H6( )
(2013·江苏,2A)
(5)戊烷(C5H12)有两种同分异构体( )
(2013·福建理综,7B)
(6)将某气体通入溴水中,溴水颜色褪去,该气体一定是乙烯( )
(2013·江苏,13C)
(7)聚乙烯塑料制品可用于食品的包装( )
(2013·四川理综,1C)
(8)聚乙烯塑料的老化是因为发生了加成反应( )
(2013·山东理综,7A)
(9)煤经过气化和液化等物理变化可转化为清洁燃料( )
(2013·山东理综,7B)
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com