
| A.锌作正极,发生氧化反应 | B.锌作负极,发生氧化反应 |
| C.锌作正极,发生还原反应 | D.锌作负极,发生还原反应 |
 夺冠金卷全能练考系列答案
夺冠金卷全能练考系列答案科目:高中化学 来源:不详 题型:单选题
| | A | B | C | D |
| 正极 | Cu | Al | Zn | Fe |
| 负极 | Zn | Zn | Cu | Zn |
| 电解质溶液 | H2SO4 | CuSO4 | ZnCl2 | CuCl2 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题

| A.Zn片为负极,Cu片为正极 | B.Zn片质量减小,电子流出 |
| C.Cu片上发生氧化反应 | D.Cu 片上有气泡产生 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题

| A.锌片是正极 |
| B.铜片上发生的反应为:Cu-2e- ="=" Cu2+[来 |
| C.电子由锌片通过导线流向铜片 |
| D.该装置能够将电能转化为化学能 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
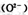 在其间通过,其工作原理如图所示。下列有关说法正确的是
在其间通过,其工作原理如图所示。下列有关说法正确的是
A.电极b为电池正极,电极反应式为 |
| B.氧化锆的作用是让电子在电池内部通过 |
C.若H2作燃料气,接触面上发生的反应为:  |
D.若CH4作燃料气,接触面上发生的反应为: 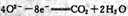 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.①③ | B.①④ | C.②③ | D.②④ |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题

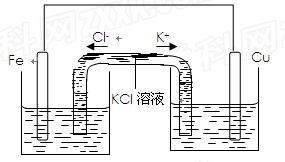
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com