
【题目】已知100℃时,水的离子积常数Kw=1×10-12,对于该温度下pH=l1的氨水,下列叙述正确的是
A. 向该溶液中加入同温同体积pH=1的盐酸,反应后溶液呈中性
B. 温度降低至25℃,该氨水溶液中H2O电离出的H+浓度小于10-11mol/L
C. 该氨水溶液中加入NH4Cl溶液,NH3·H2O的电离能力增强
D. 滴加等浓度等体积的硫酸,得到的溶液中存在电离平衡:NH4HSO4(aq)![]() NH4+(aq)+H+(aq)+SO42-(aq)
NH4+(aq)+H+(aq)+SO42-(aq)
【答案】B
【解析】已知100℃时,水的离子积常数Kw=1×10-12,对于该温度下pH=l1的氨水,c(H+)=10-11mol/L,c(OH-)=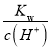 =0.1mol/L,氨水是弱碱不完全电离,物质的量浓度大于0.1mol/L。A. 向该溶液中加入同温同体积pH=1的盐酸,氨水过量,反应后溶液呈碱性,选项A错误;B. 100℃时,pH=l1的氨水中H2O电离出的H+浓度等于10-11mol/L,温度降低至25℃,氨水的电离程度减小,氢氧根离子浓度减小,抑制水的电离程度减小,则该氨水溶液中H2O电离出的H+浓度小于10-11mol/L,选项B正确;C. 该氨水溶液中加入NH4Cl溶液,铵根离子浓度增大,电离平衡逆向移动,NH3·H2O的电离能力减弱,选项C错误;D. 硫酸铵是强酸的酸式盐,是强电解质,其电离方程式为:NH4HSO4=NH4+ +H++SO42-,选项D错误。答案选B。
=0.1mol/L,氨水是弱碱不完全电离,物质的量浓度大于0.1mol/L。A. 向该溶液中加入同温同体积pH=1的盐酸,氨水过量,反应后溶液呈碱性,选项A错误;B. 100℃时,pH=l1的氨水中H2O电离出的H+浓度等于10-11mol/L,温度降低至25℃,氨水的电离程度减小,氢氧根离子浓度减小,抑制水的电离程度减小,则该氨水溶液中H2O电离出的H+浓度小于10-11mol/L,选项B正确;C. 该氨水溶液中加入NH4Cl溶液,铵根离子浓度增大,电离平衡逆向移动,NH3·H2O的电离能力减弱,选项C错误;D. 硫酸铵是强酸的酸式盐,是强电解质,其电离方程式为:NH4HSO4=NH4+ +H++SO42-,选项D错误。答案选B。


 夺冠金卷全能练考系列答案
夺冠金卷全能练考系列答案科目:高中化学 来源: 题型:
【题目】在一定体积的密闭容器中,进行如下化学反应:CO2(g)+H2(g)![]() CO(g)+H2O(g),
CO(g)+H2O(g),
其化学平衡常数K和温度t的关系如下表:
t℃ | 700 | 800 | 830 | 1000 | 1200 |
K | 0.6 | 0.9 | 1.0 | 1.7 | 2.6 |
回答下列问题:
(1)该反应的化学平衡常数表达式为K =__________________。
(2)该反应为__________反应(“吸热”或“放热”)。
(3)能判断该反应是否达到化学平衡状态的依据是_______________。
a.容器中压强不变 b.混合气体中 c(CO)不变
c.υ正(H2)=υ逆(H2O) d.c(CO2)=c(CO)
(4)某温度下,平衡浓度符合下式:c(CO2)·c(H2)=c(CO)·c(H2O),试判断此时的温度为________℃。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】t℃时,100mLNaNO3饱和溶液的质量为137g,如将这些溶液蒸干,获得62.5g NaNO3固体。下列说法中,不正确的是
A. t℃时,NaNO3饱和溶液密度为1.37g/cm3
B. t℃时,NaNO3的溶解度约为83.9g
C. t℃时,NaNO3饱和溶液中溶质的质量分数约为45.6%
D. t℃时,NaNO3饱和溶液中溶质的物质的量浓度约为1.61mol/L
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】镍氢电池具有性能好、寿命长等优点,其反应原理是NiO(OH)+ MH==NiO+M + H2O,MH可理解为储氢合金M中吸收结合氢原子,下列说法不正确的是

A. MH电极是负极
B. OH-向MH极移动
C. 正极电极反应式:NiO(OH)+e-=NiO+OH-
D. 电子从MH电极流向NiO(OH)电极,经KOH溶液流回MH极
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】向Fe和Fe2O3组成的6.56 g混合物中加入100 mL某浓度的盐酸,恰好完全反应,生成896mLH2(标准状况下),若向反应后的溶液中滴入几滴KSCN溶液,溶液不呈红色。求:
(1)原混合物中Fe2O3的质量分别为______,Fe的质量为________。
(2)原盐酸的物质的量浓度____________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在同温同压下,将充有等体积混合而成的四组气体:①NO2+O2;②NO2+NO;③HCl+N2;④SO2+O2,分别通入体积相同的试管,并立即倒立于水槽中,如图所示,待试管内液面稳定后,剩余气体体积依次V1、V2、V3、V4,则剩余气体体积最多的是( )

A. V1 B. V2 C. V3 D. V4
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列用来表示物质变化的化学用语中,正确的是( )
A. 钢铁发生电化学腐蚀的正极反应式:Fe﹣2e﹣=Fe2+
B. HS﹣的水解方程式:HS﹣+H2O![]() S2﹣+H3O+
S2﹣+H3O+
C. CO32﹣的水解方程式:CO32﹣+H2O![]() HCO3﹣+OH﹣
HCO3﹣+OH﹣
D. AlCl3溶液与Na2CO3溶液混合:2Al3++3CO32﹣=Al2(CO3)3↓
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】电渗析法是一种利用离子交换膜进行海水淡化的方法,其原理如下图所示。已知海水中含Na+、Cl-、Ca2+、Mg2+、SO42-等离子,电极为惰性电极。下列叙述中正确的是
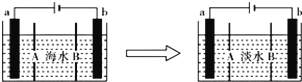
A. A膜是阳离子交换膜
B. 通电后,海水中阴离子往b电极处运动
C. 通电后,a电极的电极反应式为4OH--4e-=== O2↑+2H2O
D. 通电后,b电极上产生无色气体,溶液中出现白色沉淀
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】过氧化氢H2O2(氧的化合价为﹣1价),俗名双氧水,医疗上利用它有杀菌消毒作用来清洗伤口。对于下列A~D涉及H2O2的反应,填写空白:
A.Na2O2+2HCl===2NaCl+H2O2
B.Ag2O+H2O2===2Ag+O2+H2O
C.2H2O2===2H2O+O2
D.3H2O2+Cr2(SO4)3+10KOH===2K2CrO4+3K2SO4+8H2O
(1)H2O2仅体现氧化性的反应是_________(填代号)。
(2)H2O2既体现氧化性又体现还原性的反应是_________(填代号)。
(3)在稀硫酸中,KMnO4和H2O2能发生氧化还原反应。
氧化反应:H2O2﹣2e﹣===2H++O2↑
还原反应:MnO![]() +5e﹣+8H+===Mn2++4H2O
+5e﹣+8H+===Mn2++4H2O
写出该氧化还原反应的离子方程式:___________________。
(4)在K2Cr2O7+14HCl===2KCl+3Cl2↑+7H2O+2CrCl3的反应中,有0.3 mol电子转移时生成Cl2的体积为______(标准状况),被氧化的HCl的物质的量为____。
(5)除去镁粉中混入的铝粉杂质用溶解、_______方法,化学反应方程式为___________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com