
������ԭ��Ӧ�������������о��й㷺��;���ᴩ�Ž�
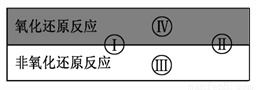
��1�����������������е��������з���������ԭ��Ӧ���� ������������ȷѡ�
A���Ŵ�����ӡˢ B��ԭ��ع��� C����е֯�� D���ҹ��Ŵ�ʪ����ͭ
��2��ˮ���������Ҫ��ɲ��֣��������к�������һ�����ʡ�
��д����ˮ�μӵķ��Ϸ�Ӧ���͢���һ����ѧ����ʽ�� ����ˮΪ ����
��3���Ȼ�麟����ں��ӡ��磺�ں���ͭ��ʱ���Ȼ�麟�ȥͭ�����������ͭ�Ա㺸�ӣ��䷴ӦΪ�� CuO+ NH4Cl = Cu+ CuCl2+ N2+ H2O
����ƽ��������ԭ��Ӧ����ʽ
�ڸ÷�Ӧ�У���������Ԫ���� ����Ԫ�����ƣ����������� ���ѧʽ��
�۷�Ӧ��������0.2mol�����壬���� ������ת�ơ�
13.��9�֣���1�� BD ��1�֣���ѡ����ѡ���÷֣���2�� 2Na + H2O = 2NaOH + H2 ����2�֣��� ���� ��1�֣������������𰸲��ո��֣���3����4 2 3 1 1 4��2�֣�ϵ��Ϊ1�����һ�֣��� �� ��1�֣��� CuO ��1�֣���1.2NA/7.2��1023��1�֣�
��������
�����������1��������Ԫ�ػ��ϼ������ķ�Ӧ����������ԭ��Ӧ������ѡ��BD�ж��漰������ԭ��Ӧ��ѡ��AC�������仯��һ������������ԭ��Ӧ����ѡBD����2�������û���Ӧ����˷��������Ŀ�����C��H2O(g) CO��H2���ڸ÷�Ӧ����Ԫ�صĻ��ϼ۽��ͣ�����ˮ������������3��������ͭ���������ԣ��������Ȼ�李��ڷ�Ӧ��ͭ�Ļ��ϼ۴ӣ�2�۽��͵�0�ۣ��õ�2�����ӡ���Ԫ�صĻ��ϼ۴ӣ�3�����ߵ�0�ۣ�ʧȥ3�����ӣ������������ͻ�ԭ�������ʵ���֮����3�U2����˷�Ӧ�ķ���ʽΪ4CuO��2NH4Cl
CO��H2���ڸ÷�Ӧ����Ԫ�صĻ��ϼ۽��ͣ�����ˮ������������3��������ͭ���������ԣ��������Ȼ�李��ڷ�Ӧ��ͭ�Ļ��ϼ۴ӣ�2�۽��͵�0�ۣ��õ�2�����ӡ���Ԫ�صĻ��ϼ۴ӣ�3�����ߵ�0�ۣ�ʧȥ3�����ӣ������������ͻ�ԭ�������ʵ���֮����3�U2����˷�Ӧ�ķ���ʽΪ4CuO��2NH4Cl 3Cu��CuCl2��N2����4H2O���ڵ�Ԫ�صĻ��ϼ����ߣ����Ա�������Ԫ���ǵ���ͭԪ�صĻ��ϼ۽��ͣ��������ͭ�����������۸��ݷ���ʽ��֪��ÿ����1mol������ת��6mol���ӣ�����������0.2
mol�����壬����1.2mol�������ɡ�ת�Ƶ�����Ϊ1.2NA/7.2��1023��
3Cu��CuCl2��N2����4H2O���ڵ�Ԫ�صĻ��ϼ����ߣ����Ա�������Ԫ���ǵ���ͭԪ�صĻ��ϼ۽��ͣ��������ͭ�����������۸��ݷ���ʽ��֪��ÿ����1mol������ת��6mol���ӣ�����������0.2
mol�����壬����1.2mol�������ɡ�ת�Ƶ�����Ϊ1.2NA/7.2��1023��
���㣺����������ԭ��Ӧ���жϺ���ƽ�͵������ļ��㡣



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�

| ||
| ||
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| A��������ʴ | B����ˮɹ�� | C��ʳ�︯�� | D��ȼ�ű��� |
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com