
| A. | NaO | B. | ZnO | C. | Na2CO3 | D. | Fe2O3 |
 优秀生应用题卡口算天天练系列答案
优秀生应用题卡口算天天练系列答案 浙江之星课时优化作业系列答案
浙江之星课时优化作业系列答案 激活思维优加课堂系列答案
激活思维优加课堂系列答案科目:高中化学 来源: 题型:选择题
| A. | 该体系中HF与CaCl2反应产生沉淀 | |
| B. | 25℃时,CaF2比CaCO3的溶解度更小 | |
| C. | 25℃时,0.1 mol•L-1 HF溶液中pH<1 | |
| D. | Ksp(CaF2)随温度和浓度的变化而变化 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 硝酸见光分解:4HNO3$\frac{\underline{\;光照\;}}{\;}$4NO2↑+O2↑+2H2O | |
| B. | 往NaOH溶液中通入过量二氧化硫:2NaOH+SO2═Na2SO3+H2O | |
| C. | SO2气体通入BaCl2溶液中产生白色沉淀:SO2+BaCl2+H2O═BaSO3↓+2HCl | |
| D. | Fe与稀H2SO4反应的化学方程式为:2Fe+3H2SO4═Fe2(SO4)3+3H2↑ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 丙烯的结构简式:C3H6 | |
| B. | Al3+能水解成Al(OH)3胶体,明矾可用作净水剂 | |
| C. | 在海轮外壳上镶入锌块,可减缓船体的腐蚀速率 | |
| D. | 盛有被KCl饱和溶液浸泡过的琼脂的U型管,可用作原电池的盐桥 |
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| 温度℃ | 25 | 80 | 230 |
| 平衡常数 | 5×104 | 2 | 1.9×10-5 |
| A. | 上述反应是熵增反应 | |
| B. | 在80℃时,测得某时刻Ni(CO)4、CO浓度均为0.5 mol•L-1,则此时反应逆向进行 | |
| C. | 25℃时,反应Ni(CO)4(g)?Ni(s)+4CO(g)的平衡常数是0.5 | |
| D. | 恒温恒容,向已达平衡的容器中再充入少量Ni(CO)4(g),达到新平衡时,CO的体积百分含量将减小 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 已知:I3-?I2+I-,向盛有KI3溶液的试管中加入适量CCl4,振荡静置后CCl4层显紫色,说明KI3在CCl4中的溶解度比在水中的大 | |
| B. | 室温下向苯和少量苯酚的混合溶液中加入适量NaOH溶液,振荡、静置后分液,可除去苯中少量苯酚 | |
| C. | “硝基苯制备”实验中,浓硫酸起到催化作用 | |
| D. | 用溴水验证裂化汽油中含有不饱和烃 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | Na2O2 和Na2O | B. | MgCl2 和Na2S | C. | CaO和CO2 | D. | HCl 和NaOH |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 四氯化碳的电子式: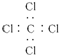 | B. | 乙醇的结构简式C2H6O | ||
| C. | 乙烯的结构简式CH2CH2 | D. | 乙炔的结构式H-C≡C-H |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com