
| ���� | HCOOH | HCN | H2CO3 |
| ����ƽ�ⳣ�� �� 25�棩 | Ki=1.77��10-4 | Ki=5.0��10-10 | Ki1=4.3��10-7 Ki2=5.6��10-11 |

���� ��1��̼ԭ�ӵijɼ������Ҫ������̼ԭ���γɹ��ۼ���ԭ�ӵ���Ŀȷ����HCN��C���γ��ĶԹ��ۼ���N���γ����Թ��ۼ���
��2���жϷǽ���ǿ���ķ����ܶ࣬�ǽ���������������ˮ���������ǿ������֤���ǽ���ǿ�����ǽ����⻯����ȶ��ԣ���˵���ǽ�����ǿ�����ǽ������������ϵ����׳̶ȣ���˵���ǽ����Ե�ǿ����
��3��NaCN��ҺpH=9��NaCNΪǿ�������Σ�ˮ��ʼ��ԣ�����ˮ��ƽ�ⳣ����������ж� K=$\frac{c��HCN��c��O{H}^{-}��}{c��C{N}^{-}��}$=$\frac{Kw}{Ka��HCN��}$=$\frac{1{0}^{-14}}{5��1{0}^{-10}}$������$\frac{c��HCN��}{c��C{N}^{-}��}$���ж���Ũ�ȴ�С��
��4����CN-�ķ�ˮ�ڴ���TiO2��������NaClO������ʹCN-ת����CNO-�������������ӣ�CNO-�����������¼�����NaClO������N2��CO2�������������ӡ�ˮ��
�ڱ���ʳ��ˮ��ȥ�Ȼ������壬ͭ��������ȥ����������̼ԭ���غ㣬�������������CN-�����ʵ�����������200mL������CN-��Ũ��0.05mol/L�����CN-�������İٷ��ʷ����жϣ�
��� �⣺��1��HCN��C���γ��ĶԹ��ۼ���N���γ����Թ��ۼ����ʽṹʽΪ��H-C��N���ʴ�Ϊ��H-C��N��
��2��a���ǽ����Ե�ǿ������̬�⻯��е��أ���a����
b������������Ӧˮ��������ǿ����Խǿ�ǽ�����Խǿ����b��ȷ��
c��Al2O3+N2+3C�T2AlN+3CO����Ӧ��CΪ��ԭ����N2Ϊ��������˵�����������Դ���̼���ʣ���˵���ǽ�����ǿ������c��ȷ��
d���ǽ����Ե�ǿ���뵥�ʾ��������أ���d����
�ʴ�Ϊ��bc��
��3��NaCN��ҺpH=9��NaCNΪǿ�������Σ�ˮ��ʼ��ԣ�CN-+H2O?HCN+OH-��PH=9����c��OH-��=10-5mol/L��ˮ��ƽ�ⳣ������Ϊ��
K=$\frac{c��HCN��c��O{H}^{-}��}{c��C{N}^{-}��}$=$\frac{Kw}{Ka��HCN��}$=$\frac{1{0}^{-14}}{5��1{0}^{-10}}$��$\frac{c��HCN��}{c��C{N}^{-}��}$=$\frac{2��1{0}^{-5}}{1{0}^{-5}}$=2��c��CN-����c��HCN����
�ʴ�Ϊ��CN-+H2O?HCN+OH-��K=$\frac{c��HCN��c��O{H}^{-}��}{c��C{N}^{-}��}$=$\frac{Kw}{Ka��HCN��}$=$\frac{1{0}^{-14}}{5��1{0}^{-10}}$��$\frac{c��HCN��}{c��C{N}^{-}��}$=$\frac{2��1{0}^{-5}}{1{0}^{-5}}$=2������
��4����CN-�ķ�ˮ�ڴ���TiO2��������NaClO������ʹCN-ת����CNO-�������������ӣ����ӷ�ӦΪCN-+ClO-�TCNO-+Cl-��CNO-�����������¼�����NaClO������N2��CO2�������������ӡ�ˮ�����ӷ�ӦΪ2CNO-+3ClO-+2H+�TN2+2CO2+3Cl-+H2O��
�ʴ�Ϊ��CN-+ClO-=CNO-+Cl-��2CNO-+3ClO-+2H+�TN2+2CO2+3Cl-+H2O��
���������ɵ������N2��CO2�⣬����HCl��������Cl2�ȣ�
��A������ʳ��ˮ�ܹ���ȥ�Ȼ������ʣ���A��ȷ��
��B������NaHCO3��Һ���Ȼ��ⷴӦ���ɶ�����̼�Զ�����̼�IJⶨ����B����
��C��ŨNaOH��Һ�������Ȼ���Ͷ�����̼�����ܲⶨCO2������ȷ��CN-�Ĵ���Ч������C����
��D��Ũ����������Ȼ��⣬�Բⶨ������̼����Ӱ�죬��D����
��ѡA��
ͭ���ܹ���������Ӧ�Ӷ���ȥ�������ʣ�����ʵ���е������dz�ȥ���������Cl2����ֹ��CO2�ⶨ����Ӱ�죬
200mL������CN-��Ũ��0.05mol/L�����Һ�к��е�CN-�����ʵ����ǣ�0.2L��0.05mol/L=0.01mol������̼ԭ���غ㣬��������0.01mol������̼������ʯ��ˮ���������ɵ�̼��Ƶ����ʵ����ǣ�0.0082mol����Ӧ��CN-�����ʵ�����0.0082mol��CN-�������İٷ����ǣ�$\frac{0.0082mol}{0.01mol}$��100%=82%��80%��
�ʴ�Ϊ��A����ȥ���������Cl2����ֹ��CO2�ⶨ����Ӱ�죬����
���� ���⿼����������ʵ���ƽ�⡢����ˮ�⡢�������Ǹ߿��еij������ͣ������е��Ѷȵ����⣬�����ۺ���ǿ�����ض�ѧ��������������ѵ��������������ѧ���淶�Ͻ���ʵ����ơ���������������������ԭ��Ӧ����ʽ��д�Ŀ��飬ע���жϷ�����������ԭ��Ӧ����Ŀ�ѶȲ���



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | �������Ż�ʱʹ����ĭ�������� | |
| B�� | ���Թܼ���̼�����ƹ���ʱʹ�Թܿ���ֱ���� | |
| C�� | Ũ���ὦ��Ƥ����ʱ������ϡ����������Һ��ϴ | |
| D�� | ����ʱӦ������������ͨ������ˮ�ټ��� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | x+y��3 | |
| B�� | ��Ӧ���ʼӿ죬����Ӱٷ������� | |
| C�� | A��ת���ʼ�С������������� | |
| D�� | ƽ�������ƶ���ƽ�ⳣ������ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
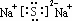 ����ˮ��Һ������Ũ���ɴ�С��˳����c��Na+����c��S2-����c��OH-����c��HS-����c��H+����
����ˮ��Һ������Ũ���ɴ�С��˳����c��Na+����c��S2-����c��OH-����c��HS-����c��H+�����鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
| ʱ��/min | 0 | 15 | 30 | 45 | 60 | 90 | 120 | |
| ��ֽ�� ��ɫ �仯 | ����Ƭ���� �ϵ���ֽ | ��ɫ | ��ɫ | ��ɫ | dz��ɫ | ��ɫ | ��ɫ | dz��ɫ |
| ����Ƭ���� �ϵ���ֽ | ��ɫ | ��ɫ | ��ɫ | ��ɫ | ��ɫ | ��ɫ | dz��ɫ | |
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com