
 +H+=
+H+=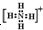 ;由5个原子核10个电子组成的化合物电子式是
;由5个原子核10个电子组成的化合物电子式是 ,结构式是
,结构式是 .
. 分析 由2个原子核10个电子组成的化合物分子式是 HF,结构式是 H-F;由3个原子核10个电子组成的化合物分子式是H2O,水为共价化合物,氧原子最外层8个电子,分子中存在两个氧氢键,结构式是H-O-H;由4个原子核10个电子组成的化合物是NH3名称是氨气,用电子式表示氨气与质子结合的化学反应过程;由5个原子核10个电子组成的化合物是CH4,根据1个甲烷分子中含1个C、4个H原子,为正四面体,键角为109°28′,碳原子最外层有4个电子,能形成4个共价键达到稳定结构,每个氢原子能形成一个共价键达到稳定结构,据此写出甲烷的电子式与结构式,电子式 .结构式
.结构式 .
.
解答 解:由2个原子核10个电子组成的化合物分子式是 HF,结构式是 H-F;
由3个原子核10个电子组成的化合物分子式是H2O,水为共价化合物,氧原子最外层8个电子,分子中存在两个氧氢键,结构式是 H-O-H;
由4个原子核10个电子组成的化合物是NH3名称是氨气,用电子式表示氨气与质子结合的化学反应过程: +H+=
+H+=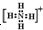 ;
;
由5个原子核10个电子组成的化合物是CH4,根据1个甲烷分子中含1个C、4个H原子,为正四面体,键角为109°28′,碳原子最外层有4个电子,能形成4个共价键达到稳定结构,每个氢原子能形成一个共价键达到稳定结构,据此写出甲烷的电子式与结构式,电子式 .结构式
.结构式 ,
,
故答案为:HF;H-F;H2O;H-O-H;氨气; +H+=
+H+=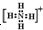 ;
; ;
; .
.
点评 本题考查了学生对于10电子体的熟悉程度,电子式和结构式的书写、用电子式表示形成过程,题目难度中等,试题的题量较大,要求学生熟练掌握电子式的概念及表示方法.


科目:高中化学 来源: 题型:选择题
| A. | 中国古代利用明矾溶液的酸性清除铜镜表面的铜锈 | |
| B. | 氢氧化铝可作抗酸药 | |
| C. | 碘是人体必需微量元素,所以要多吃富含高碘酸的食物 | |
| D. | 硅胶可用作食品干燥剂 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | Al(OH)3分解的产物可用于制备金属铝 | |
| B. | 电解熔融氯化钠所得到的金属钠呈液态 | |
| C. | MgO的熔点很高,可用于制作耐高温材料 | |
| D. | 电解MgCl2水溶液,可制得金属镁 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 1 mol N4分子的质量是56 g | |
| B. | 标况下,NA个 H2O分子含有3NA个原子 | |
| C. | 常温下,1 mo/L 的NH4Cl 溶液中NH4+的浓度小于1 mol/L | |
| D. | 高温高压,催化剂条件下,28 g N2分子与6 g H2充分反应可生成34 g NH3 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 分子数之比为1:1 | B. | 原子数之比为1:1 | C. | 原子数之比为3:2 | D. | 物质的量之比2:3 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:推断题
查看答案和解析>>
科目:高中化学 来源: 题型:计算题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com