

| ||
| ||
| m |
| M |
| 102g |
| 102g/mol |
| 3 |
| 2 |
| ||
| ||


 口算心算速算应用题系列答案
口算心算速算应用题系列答案 同步拓展阅读系列答案
同步拓展阅读系列答案科目:高中化学 来源: 题型:
 W、X、Y、Z是四种常见的短周期元素,其原子半径随原子序数变化如下图所示.已知W的一种核素的质量数为18,中子数为10;X和Ne原子的核外电子数相差1;Y的单质是一种常见的半导体材料;Z的非金属性在同周期主族元素中最强.下列说法正确的是( )
W、X、Y、Z是四种常见的短周期元素,其原子半径随原子序数变化如下图所示.已知W的一种核素的质量数为18,中子数为10;X和Ne原子的核外电子数相差1;Y的单质是一种常见的半导体材料;Z的非金属性在同周期主族元素中最强.下列说法正确的是( )| A、X位于元素周期表中第2周期第ⅦA族 |
| B、W元素的最高正价等于它的主族序数 |
| C、X的单质与Y的单质相比,熔点较高的是X |
| D、Z元素的气态氢化物的沸点在同主族元素的气态氢化物中最低 |
查看答案和解析>>
科目:高中化学 来源: 题型:
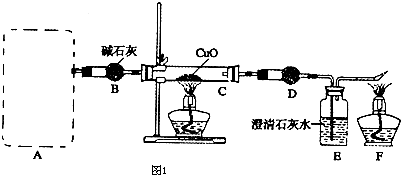
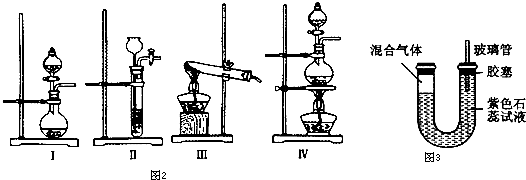
查看答案和解析>>
科目:高中化学 来源: 题型:
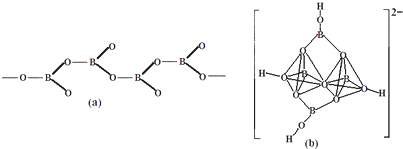
查看答案和解析>>
科目:高中化学 来源: 题型:

查看答案和解析>>
科目:高中化学 来源: 题型:
| A、利用太阳能等清洁能源代替化石燃料,有利于节约资源、保护环境 |
| B、催化转化机动车尾气为无害气体,能消除酸雨和雾霾的发生 |
| C、研发高效低毒的农药,降低蔬菜的农药残留量 |
| D、积极开发废电池的综合利用技术,防止电池中的重金属等污染土壤和水体 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、pH=3的盐酸与pH=11的氨水 |
| B、等物质的量浓度的盐酸与氢氧化钾溶液 |
| C、等物质的量浓度的醋酸与氢氧化钠溶液 |
| D、pH=3的醋酸与pH=11的氢氧化钠溶液 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com