
【题目】甲、乙、丙、丁均为中学化学常见的纯净物,它们之间有如下图所示的反应关系。下列物质组不满足上述转化关系的是( )

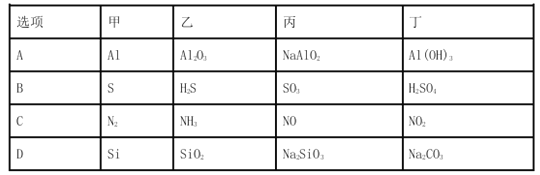
A. A B. B C. C D. D
 小题狂做系列答案
小题狂做系列答案科目:高中化学 来源: 题型:
【题目】配位化合物的数量巨大,组成和结构形形色色,丰富多彩。配合物[Cu(NH3)4](OH)2的中心离子、配体、中心离子的电荷数和配位数分别为
A.Cu2+、NH3、+2、4 B.Cu+、NH3、+1、4
C.Cu2+、OH-、+2、2 D.Cu2+、NH3、+2、2
答
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】H2O2不稳定、易分解,Fe3+、Cu2+等对其分解起催化作用,为比较Fe3+和Cu2+对H2O2分解的催化效果,某化学研究小组同学分别设计了甲、乙两种实验装置。


(1)若利用甲实验,可通过观察__________________________现象,从而定性比较得出结论。有同学提出将FeCl3改为Fe2(SO4)3更为合理,其理由是_____________________________,写出H2O2在二氧化锰催化作用下发生反应的化学方程式:__________________________,若利用乙实验可进行定量分析,图中仪器A的名称为________________,实验时均以生成40 mL气体为准,其他可能影响实验的因素均已忽略,实验中还需要测量的数据是_____________。
(2)将0.1 mol MnO2粉末加入50 mL H2O2溶液中,在标准状况下放出气体的体积和时间的关系如图所示,解释反应速率变化的原因:________________________________,H2O2初始物质的量浓度为__________(保留两位有效数字)。

(3)为了加深同学们对影响反应速率因素的认识,老师让同学完成如下实验:在上述实验装置的锥形瓶内加入6.5 g锌粒,通过分液漏斗加入40 mL 2.5 mol·L-1的硫酸,10s时收集产生的H2的体积为44.8 mL(标准状况),用硫酸表示10 s内该反应的速率为________ mol·L-1·s-1(假设反应前后溶液的体积不变)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列物质的分离方法错误的是
A.采用蒸发法从食盐水中提取食盐
B.用结晶法除去硝酸钾中的氯化钠
C.用酒精从溴水中萃取溴
D.用分液法分离汽油和水的混合物
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在相同温度下,有相同体积的甲、乙两容器,甲容器中充入1g N2和1g H2,乙容器中充入2g N2和2g H2。下列叙述中,错误的是
A. 化学反应速率:乙>甲 B. 平衡后N2的浓度:乙>甲
C. H2的转化率:乙>甲 D. 平衡混合气中H2的体积分数:乙>甲
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列各组离子,能在溶液中大量共存的是( )
A. Al3+、Na+、HCO3-、OH- B. Na+、Fe2+、H+、NO3-
C. K+、Fe3+、SCN-、SO32- D. Na+、Ag+、H+、NO3-
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】现有浓度均为 0.1 mol·L-1 的下列溶液: ①硫酸 ②醋酸 ③氢氧化钠
请回答下列问题:
(1)三种溶液中由水电离出的 H+浓度由大到小的顺序是(填序号)____________。
(2)已知 T ℃, KW=1×10-13,则 T ℃_________25 ℃(填“>”、 “<”或“=”)。在 T ℃时将pH=11的NaOH溶液a L与 pH=1的硫酸b L混合(忽略混合后溶液体积的变化),若所得混合溶液的pH=10,则 a∶b=____________。
(3) 25 ℃时,有 pH=x 的盐酸和 pH=y 的氢氧化钠溶液(x≤6, y≥8),取 a L 该盐酸与 b L该氢氧化钠溶液反应,恰好完全中和,求:
①若 x+y=14,则 a/b=____________(填数据);
②若 x+y=13,则 a/b=____________(填数据);
③若 x+y>14,则 a/b=____________(填表达式);
④该盐酸与该氢氧化钠溶液完全中和,两溶液的 pH 满足关系____________(用 x、 y 表示)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】将8 mL NO2和O2的混合气体通入倒立于水槽中装满水的量筒,充分反应后,剩余气体为1 mL,则原混合气体中NO2和O2的体积比可能为 ( )
A. 7∶5 B. 3∶7 C. 7∶1 D. 1∶7
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氮及其化合物广泛存在于自然界中,回答下列问题:
(1)在基态16N中,其s能电子云形状是_____形的,其p能级轨道上存在______个自旋方向相同的电子;CN-中共价键的类型有______。
(2)碱性肥料氰氮化钙(CaCN2)的组成元素第一电离能最小的是_______(填名称)。
(3)化合物(CH3)3N能溶于水,其原因是_______________,(CH3)3N与盐酸反应生成[(CH3)3NH]+,该过程新生成的化学键类型为__________________.。
(4)阳离子[(CH3)3NH]+和阴离子A可按个数比4:1组成化合物,阴离子A的结构如图1所示,则S原子的杂化轨道类型是______,阴离子A的化学式为______。

(5)立方氮化硼的晶胞如图2所示(白球为氮原子,黑球为硼原子),则硼原子的配位数为______;若晶胞边长为acm,则立方氮化硼的密度是______g·cm-3(只要求列算式,阿伏伽德罗常数用NA表示)。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com