
【题目】【化学-物质结构与性质】氮的化合物在无机化工领域有着重要的地位。请回答下列问题:
(1)基态氮原子的价电子排布图为 。
(2)氮的最高价氧化物为无色晶体,它由两种离子构成:已知其阴离子构型为平面正三角形,则其阳离子的构型为 形,阳离子中氮的杂化方式为 。
(3)某氮铝化合物X具有耐高温、抗冲击、导热性好等优良性质,广泛用于陶瓷工业等领域。工业上用氮气、氧化铝和碳在一定条件下反应生成CO和X (X的晶体结构如图所示),工业制备 X 的化学方程式为 。

(4)X晶体中包含的化学键类型为 (填字母标号)。
A .离子键 B .共价键 C .配位键 D .金属键
(5)已知氮化硼与X晶体类型相同,且氮化硼的熔点比X高,其原因是 。
(6)若X的密度为ρg/cm3,则晶体中最近的两个Al 原子的距离为 cm (阿伏加德罗常数用 NA表示,不必化简)。
【答案】(1)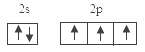 ;
;
(2)直线,sp;
(3)Al2O3+N2+3C![]() 2AlN+3CO;(4)BC;
2AlN+3CO;(4)BC;
(5)氮化硼与氮化铝均为原子晶体,且硼原子半径小于铝原子半径,B—N键键能大于Al—N键键能;
(6)
【解析】
试题分析:(1)7号元素N的基态氮原子的价电子排布图为 ;
;
(2)氮的最高价氧化物为无色晶体,它由两种离子构成:已知其阴离子构型为平面正三角形,则其阳离子的构型为直线形;阳离子中氮的杂化方式为sp杂化;
(3)某氮铝化合物X具有耐高温、抗冲击、导热性好等优良性质,广泛用于陶瓷工业等领域。工业上用氮气、氧化铝和碳在一定条件下反应生成CO和X (X的晶体结构如图所示),工业制备 X 的化学方程式为Al2O3+N2+3C![]() 2AlN+3CO;
2AlN+3CO;
(4)根据X晶体结构示意图可知:在X中包含的化学键类型为共价键、配位键,答案选B、C;
(5)已知氮化硼与X晶体类型相同,且氮化硼的熔点比X高,其原因是氮化硼与氮化铝均为原子晶体,且硼原子半径小于铝原子半径,B—N键键能大于Al—N键键能,断裂共价键消耗的能量高;
(6)若X的密度为ρg/cm3,在晶体中最近的两个Al 原子的距离为晶胞的面对角线的一半,在每个晶胞中含有Al:8×1/8+6×1/3=4,含有N:4个,即在一个晶胞中含有4个AlN,根据密度计算公式ρ=![]() 可得V=m÷ρ=
可得V=m÷ρ=![]() ,所以晶胞的边长L=
,所以晶胞的边长L= ,则晶体中最近的两个Al 原子的距离为a=
,则晶体中最近的两个Al 原子的距离为a= 。
。


 阳光课堂课时作业系列答案
阳光课堂课时作业系列答案科目:高中化学 来源: 题型:
【题目】某高校老师要求学生配制0.1 mol/L的KMnO4溶液100mL。完成下列实验。
【实验一】研究温度对反应速率的影响,学生取两只试管,均加入4mL 0.1 mol/L的KMnO4酸性溶液和10mL 0.1mol/L H2C2O4(乙二酸)溶液,振荡,A试管置于热水中,B试管置于凉水中,记录溶液褪色所需的时间。要用 来酸化KMnO4溶液,褪色所需时间tA tB(填“>”、“=”或“<”)。写出此反应的离子方程式: 。
【实验二】测定某乙二酸溶液的浓度,具体操作为:
(1)滴定:准确量取25.00 mL乙二酸溶液于锥形瓶中,加少量酸酸化,将KMnO4溶液装入________(填“酸式”或“碱式”)滴定管,进行滴定操作。在实验中发现,刚滴下少量KMnO4溶液时,溶液迅速变成紫红色。将锥形瓶摇动一段时间后,紫红色慢慢消失;再继续滴加时,紫红色就很快褪色了。
请解释原因: 。待到 ,证明达到滴定终点。
(2)计算:再重复上述操作2次,记录实验数据如下。
序号 | 滴定前读数(mL) | 滴定后读数(mL) |
1 | 0.00 | 20.10 |
2 | 1.00 | 20.90 |
3 | 0.00 | 22.10 |
则此乙二酸溶液的浓度为 。
(3) 误差分析:下列操作会导致乙二酸溶液浓度偏高的是 。
A. 配制KMnO4溶液定容时,仰视观察刻度线
B.未用待测液乙二酸润洗滴定管
C.滴定前锥形瓶有少量水
D.滴定前滴定管尖嘴部分有气泡,滴定后气泡消失
E.滴定时振荡锥形瓶有溶液飞溅出去
F.观察读数时,滴定前仰视,滴定后俯视
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】构成DNA、唾液淀粉酶、固醇、纤维素的化学成分中,共有的化学元素是
A. C、H、0、N、P B. C、H、0、N、S
C. C、H、0 D. C、H、0、N
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】〔化学-化学与技术〕
工业中以铝土矿(主要成分为Al2O3,另含有Fe2O3和SiO2)为原料冶炼铝过程如图所示:

(1) 实验室进行过滤用到的玻璃仪器有烧杯、_____________、_____________。
(2) 操作II中生成不溶物C的离子方程式是 。
(3) 氧化铝的熔点高达2050℃,工业上为降低能耗,在铝的电解冶炼时,采取的措施是 。
(4) 电解冶炼铝时,阳极和阴极以碳素材料制成,电解过程中,阳极材料需定期进行更换,原因是 。
(5) 为了提高综合经济效益,实际工业生产中常将上述反应中的相关物质循环利用。其部分转化关系如下图所示:
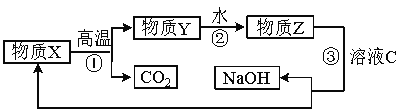
① 上述转化中未涉及四种基本反应类型中的 反应;
② 写出过程③的化学方程式: 。
(6) 研究表明,人体过量吸入铝元素会严重危害身体健康。请你结合实际提出两条杜绝铝元素过量吸入的措施:____________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列反应中属于氧化还原反应,但水既不作氧化剂又不作还原剂的是( )
A.SO3+H2O===H2SO4
B.2Na2O2+2H2O===4NaOH+O2↑
C.2F2+2H2O===4HF+O2
D.2Na+2H2O===2NaOH+H2↑
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】配平下列化学方程式或离子方程式。
(1)![]() KI+
KI+![]() KIO3+
KIO3+![]() H2SO4=
H2SO4=![]() I2+
I2+![]() K2SO4+
K2SO4+![]() H2O
H2O
(2)![]() MnO+
MnO+![]() H++
H++![]() Cl-=
Cl-=![]() Mn2++
Mn2++![]() Cl2↑+
Cl2↑+![]() H2O
H2O
(3)![]() P4+
P4+![]() KOH+
KOH+![]() H2O=
H2O=![]() K3PO4+
K3PO4+![]() PH3
PH3
(4)![]() ClO-+
ClO-+![]() Fe(OH)3+
Fe(OH)3+![]() ________=
________=![]() Cl-+
Cl-+![]() FeO+
FeO+![]() H2O
H2O
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图所示:

下列说法正确的是
A.甲池通入O2的电极反应为O2 + 4e-+ 4H+=2H2O
B.乙池 Ag电极增重6.4g,溶液中将转移0.2mol电子
C.反应一段时间后,向乙池中加入一定量Cu(OH)2固体,能使CuSO4溶液恢复到原浓度
D.甲池中消耗280 mL(标准状况下)O2,此时丙池中理论上最多产生1.45g固体
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列有关实验的说法错误的是
A. 将一小块试纸放在表面皿上,用玻璃棒蘸取少量待测液点在试纸上,再与标准比色卡对照
B. 无色溶液中加Ba(NO3)2溶液,再加稀盐酸,沉淀不溶解,不能说明原溶液中一定有SO42-
C. 蒸馏时蒸馏烧瓶中液体的体积不能超过容积的![]() ,液体也不能蒸干
,液体也不能蒸干
D. 将固体加入容量瓶中溶解并稀释至刻度,配制成一定物质的量浓度的溶液
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知:反应①Fe(s)+CO2(g) ![]() FeO(s)+CO(g) ΔH1 的平衡常数为K1;
FeO(s)+CO(g) ΔH1 的平衡常数为K1;
反应②Fe(s)+H2O(g) ![]() FeO(s)+H2(g) ΔH2 的平衡常数为K2。
FeO(s)+H2(g) ΔH2 的平衡常数为K2。
反应③CO2(g)+H2(g) ![]() CO(g)+H2O(g) ΔH3 的平衡常数为K3。
CO(g)+H2O(g) ΔH3 的平衡常数为K3。
不同温度时K1、K2的值如下表,下列说法正确的是 ( )
温度/K | K1 | K2 |
973 | 1.47 | 2.38 |
1 173 | 2.15 | 1.67 |
A.K3= K1-K2 B.K3= K1+ K2 C.ΔH3 > 0 D.ΔH3 < 0
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com