
| A. | 100kg | B. | 160kg | C. | 240kg | D. | 300kg |
分析 根据c=$\frac{1000ρω}{M}$计算出M(C2H4O2)=60g•mol-1,物质的量浓度为0.945mol•L-1优质醋酸(C2H4O2)质量分数;根据优质醋的质量分数计算出醋酸的质量,然后根据半成醋与优质醋中醋酸的质量相等计算出半成醋的总质量,从而得出需捞出的冰和蒸发的水总质量.
解答 解:根据c=$\frac{1000ρω}{M}$可知,ω=$\frac{cM}{1000ρ}$$\frac{0.945×60}{1.050×1000}$=5.4%,
300kg优质醋中含有醋酸的质量为:300kg×5.4%=16.2kg,
用含醋酸(C2H4O2)质量分数为3%的半成醋制取优质醋的过程中,醋酸的质量不变,则原半成醋的总质量为:$\frac{16.2kg}{3%}$=540kg,
所以需捞出的冰和蒸发的水总质量为:540kg-300g=240kg,
故选C.
点评 本题考查了物质的量浓度的计算,题目难度中等,正确分析题干信息为解答关键,注意掌握物质的量浓度与溶质质量分数之间的关系,试题培养了学生的分析能力及化学计算能力.


 名师导航单元期末冲刺100分系列答案
名师导航单元期末冲刺100分系列答案 名校名卷单元同步训练测试题系列答案
名校名卷单元同步训练测试题系列答案科目:高中化学 来源: 题型:解答题
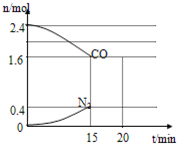 CO和NO是汽车尾气的主要污染物.消除汽车尾气的反应式之一为:2NO(g)+2CO(g)?N2(g)+2CO2(g).请回答下列问题:
CO和NO是汽车尾气的主要污染物.消除汽车尾气的反应式之一为:2NO(g)+2CO(g)?N2(g)+2CO2(g).请回答下列问题:查看答案和解析>>
科目:高中化学 来源: 题型:填空题
| 族 周期 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅤⅡA | 0 |
| 二 | ① | ② | ③ | ④ | ||||
| 三 | ⑤ | ⑥ | ⑦ | ⑧ |
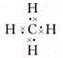 .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 6.02×1023个碳原子的质量为1 g | |
| B. | 钠原子的摩尔质量为23 g | |
| C. | HCl的摩尔质量等于6.02×1023个HCl分子的质量 | |
| D. | Na2O2的摩尔质量为78 g/mol |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
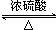 CH3COOC2H5+H2O.
CH3COOC2H5+H2O.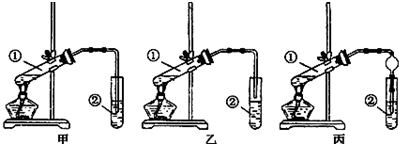
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 蛋白质、淀粉和油脂都属于高分子化合物 | |
| B. | 人造纤维.合成纤维.碳纤维.光导纤维主要成分都是纤维素 | |
| C. | 误食重金属盐类时,可以喝大量牛奶、蛋清或豆浆解毒 | |
| D. | 福尔马林主要成分是甲酸,由于可使蛋白质变性,可用于保存动物标本 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
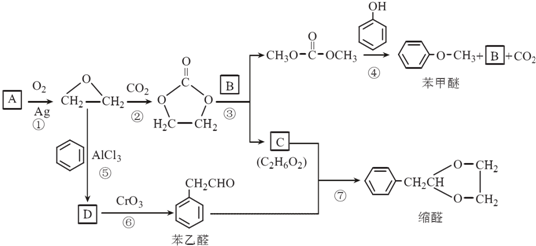
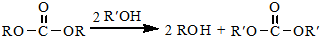
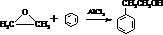 .
.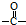 结构,核磁共振氢谱有4组峰,峰面积之比为3:2:2:1.
结构,核磁共振氢谱有4组峰,峰面积之比为3:2:2:1.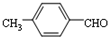 ,
,
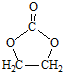 的合成路线,设计一条由2-氯丙烷和必要的无机试剂制备
的合成路线,设计一条由2-氯丙烷和必要的无机试剂制备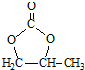 的合成路线(注明必要的反应条件).
的合成路线(注明必要的反应条件).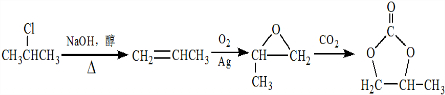 .
.查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com