
【题目】某小组同学利用如图所示装置探究二氧化硫气体的性质. 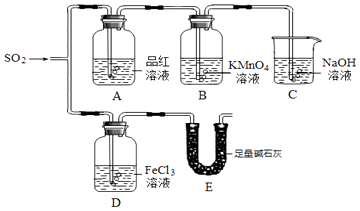
请回答:
(1)仪器E的名称是 . 若没有装置C,将气体直接排放到空气中,会带来的主要环境问题是 .
(2)观察到B中溶液颜色变浅,说明了SO2具有的性质是;
(3)写出仪器D中的实验现象 , 发生氧化还原反应的离子方程式 .
科目:高中化学 来源: 题型:
【题目】氯化铁溶液与氢氧化铁胶体具有的共同性质是
A. 分散质粒子直径都在1—100nm之间 B. 都能透过半透膜
C. 都能通过滤纸 D. 都能产生丁达尔效应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知某强氧化剂[RO(OH)2]2+离子2.4×10-3mol被亚硫酸钠还原到较低价态,需12mL0.2mol/L的亚硫酸钠溶液,则反应后R的化合价为( )
A.0B.+2C.+3D.+4
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氯元素的单质及其化合物在生产生活中应用极其广泛.请完成下列填空: 
(1)氯气性质探究
设计如图实验装置来制备并验证氯气的性质(部分夹持装置未画出).
(i)A中放置固体二氧化锰的装置名称是 .
(ii)装置B的作用是 .
(iii)硬质玻璃管C中事先装有两个沾有相关试剂的棉球,左侧棉球的实验现象为 .
(iv)D中的NaOH溶液用来吸收尾气,向反应后的D中加入足量稀硫酸会产生气体,写出该反应的离子方程式 .
(2)制备HClO
设计装置E代替如图的装置C,用于制备较高浓度的HClO溶液.在圆底烧瓶底部,有一用塑料网包住的过量块状碳酸钙.
①该方案可以制得较高浓度HClO的原因是(结合必要的化学语言回答) .
②反应结束后将塑料网中剩余的石灰石提出液面,所得的溶液与稀盐酸混合,立即产生大量CO2气体,则反应所得溶液中的溶质除HClO外,还含有、(写两种钙盐的化学式,一种正盐,一种酸式盐);该小组同学测得反应中碳酸钙质量减少M g,反应后从所得的200mL溶液中取用10mL与足量稀盐酸混合,连接F装置测得产生的气体体积为V L(已换算成标准状况),则原溶液中含钙正盐的浓度为molL﹣1(用含M、V的代数式表示).
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】到目前为止,由化学能转变的热能或电能仍然是人类使用最主要的能源.
(1)化学反应中放出的热能(焓变,△H)与反应物和生成物的键能(E)有关.已知:H2(g)+Cl2(g)=2HCl(g)△H=﹣a kJmol﹣1;E(H﹣H)=b kJmol﹣1 , E(Cl﹣Cl)=c kJmol﹣1 , 则:E(H﹣Cl)=;
(2)氯原子对O3的分解有催化作用:O3(g)+Cl(g)=ClO(g)+O2(g)△H1 , ClO(g)+O(g)=Cl(g)+O2(g)△H2 , 大气臭氧层的分解反应是O3+O=2O2△H.该反应的能量变化示意图如图1所示.则反应O3(g)+O(g)=2O2(g)的正反应的活化能为kJmol﹣1 . 
(3)实验中不能直接测出由石墨和氢气反应生成甲烷反应的反应热,但可测出CH4、石墨和H2燃烧反应的反应热,求由石墨生成甲烷的反应热.已知:
①CH4(g)+2O2(g)═CO2(g)+2H2O(l)△H=﹣a kJmol﹣1
②C(石墨)+O2(g)═CO2(g)△H=﹣b kJmol﹣1
③H2(g)+ ![]() O2(g)═H2O(l)△H=﹣c kJmol﹣1
O2(g)═H2O(l)△H=﹣c kJmol﹣1
则反应C(石墨)+2H2(g)→CH4(g)的反应热:
△H=kJmol﹣1 .
又已知:该反应为放热反应,△H﹣T△S可作为反应方向的判据,当△H﹣T△S<0时可自发进行;则该反应在什么条件下可自发进行 . (填“低温”、“高温”)
(4)有图2所示的装置,该装置中Cu极为极;当铜片的质量变化为12.8g时,a极上消耗的O2在标准状况下的体积为L. 
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图所示,装置(Ⅰ)是一种可充电电池,装置(Ⅱ)为电解池,装置(Ⅰ)的离子交换膜只允许Na+通过.电池充、放电的化学方程式为:
2Na2S2+NaBr3 ![]() Na2S4+3NaBr,当闭合K时,X极附近溶液变红色.
Na2S4+3NaBr,当闭合K时,X极附近溶液变红色.
下列说法正确的是( )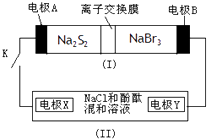
A.装置(I)中Na+从右到左通过离子交换膜
B.A电极的电极反应式为:NaBr3+2Na++2e﹣=3NaBr
C.X电极的电极反应式为:2Cl﹣﹣2e﹣=Cl2↑
D.每有0.1mol Na+通过离子交换膜,X电极上就生成标准状况下气体1.12L
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com